Потенційні антиоксиданти ізолятів вторинного метаболіту фракції етилацетату з листя Coleus amboinicus Lour.
DOI:
https://doi.org/10.15587/2519-4852.2022.266401Ключові слова:
вторинні метаболіти, Coleus amboinicus Lour., DPPH, ацетоксигормінонАнотація
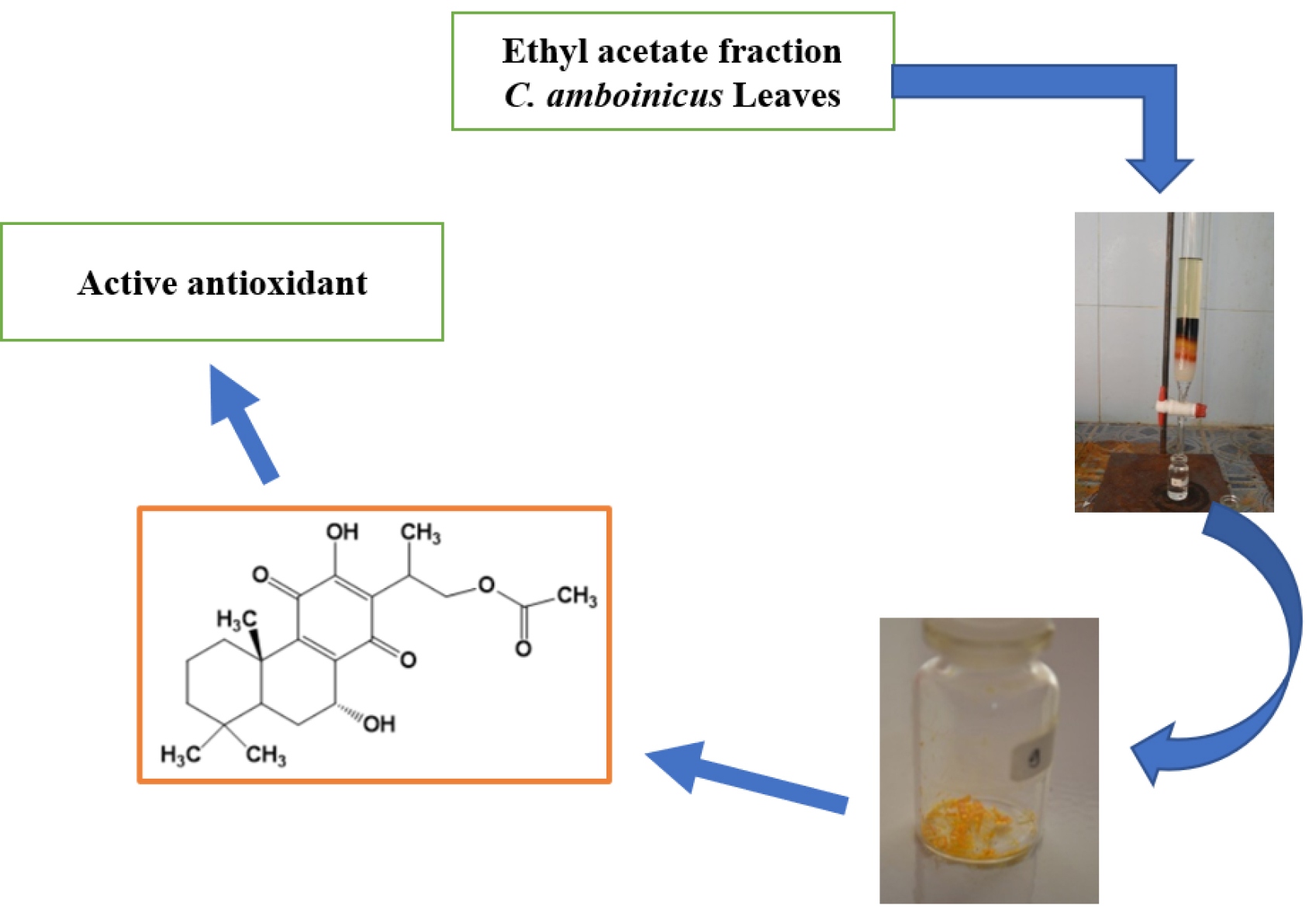
Метою дослідження було виділити та охарактеризувати вторинні метаболіти, які мають потенціал як антиоксиданти, з етилацетатної фракції листя Coleus amboinicus, L. (C. amboinicus).
Матеріали та методи. Очищення етилацетатної фракції C. amboinicus за допомогою гравітаційної колонкової хроматографії з нерухомою фазою (силікагель, Merck) і рухомою фазою із співвідношенням розчинників н-гексан (Merck) і етилацетат (Merck). Дослідження ізолятів включає фізичні характеристики (колір, форма та температура плавлення). Якісне визначення чистоти за допомогою ТШХ проводилося при довжинах хвиль 254 нм і 366 нм. Структурний аналіз метаболітів проведений за допомогою УФ-видимого спектрометра (Spectronic 3000, Genesis 10, Японія), FT-IR (KBr) (Shimadzu IR Prestige-21, Японія), ЯМР-спектрометра (спектрометр JEOL, Японія), що працює на частоті 500 МГц (1H- ЯМР) і 125 МГц (13C-ЯМР), а також GC-MS Shimadzu (QP-2010S Shimadzu, Японія) і визначення потенційної антиоксидантної активності за допомогою методу DPPH.
Результати. Сполуки вторинного метаболіту виділяли у вигляді жовтих кристалів з температурою плавлення 232-233 °С, значеннями Rf 0,86 і 0,56, які контролювали за допомогою ТШХ при співвідношенні розчинників н-гексан і етилацетат 6:4 і 8:2. Спектронний аналіз за допомогою спектрометра UV-Vis показав два електронні поглинання, а саме довжину хвилі 210 нм, що вказує на метанол як розчинник, і 272 нм для ізоляту. Поглинання функціональних груп при хвильових числах 3379 см-1 (-OH; гідрокси), 2931 см-1 (-CH; аліфатична), 1735 см-1 (-C=O; карбонілкетон), 1234 см-1 (-CO-; метокси) і 1643 см-1 (-C=C-; алкен). ГХ-МС аналіз дав два піки абсорбції: (1) перший час утримування 6,658 хвилин (3,95 %) і (2) другий час утримування 9,001 хвилин (96,05 %). Структурний аналіз за допомогою 1H&13C-ЯМР показав наявність 28 типів протонів і 22 типи вуглецю. Тест потенціалу антиоксидантної активності показав значення активності (IC50) 338,54 ppm.
Висновок. Структура ізольованої вторинної метаболічної сполуки являє собою 16-ацетокси-7α-гідроксиройлеанон (син. 16-ацетоксигормінон) і має потенціал як антиоксидант.
Посилання
- Gupta, N., Verma, K., Nalla, S., Kulshreshtha, A., Lall, R., Prasad, S. (2020). Free Radicals as a Double-Edged Sword: The Cancer Preventive and Therapeutic Roles of Curcumin. Molecules, 25 (22), 5390. doi: https://doi.org/10.3390/molecules25225390
- Mahantesh, S. P., Gangawane, A. K., Patil, C. S. (2021). Free Radicals, Antioxidants, Diseases and Phytomedicines in Human Health: Future Rerspects. World Research Journal of Medicinal & Aromatic Plants, 1 (1), 6–10.
- Sharma, G. N., Gupta, G., Sharma, P. (2018). A Comprehensive Review of Free Radicals, Antioxidants, and Their Relationship with Human Ailments. Critical Reviews in Eukaryotic Gene Expression, 28 (2), 139–154. doi: https://doi.org/10.1615/critreveukaryotgeneexpr.2018022258
- Pervin, M., Hasnat, Md., Lee, Y., Kim, D., Jo, J., Lim, B. (2014). Antioxidant Activity and Acetylcholinesterase Inhibition of Grape Skin Anthocyanin (GSA). Molecules, 19 (7), 9403–9418. doi: https://doi.org/10.3390/molecules19079403
- Jamshidi-kia, F., Wibowo, J. P., Elachouri, M., Masumi, R., Salehifard-Jouneghani, A. et al. (2020). Battle between plants as antioxidants with free radicals in human body. Journal of Herbmed Pharmacology, 9 (3), 191–199. doi: https://doi.org/10.34172/jhp.2020.25
- Amorati, R., Valgimigli, L. (2018). Methods To Measure the Antioxidant Activity of Phytochemicals and Plant Extracts. Journal of Agricultural and Food Chemistry, 66 (13), 3324–3329. doi: https://doi.org/10.1021/acs.jafc.8b01079
- Lourenço, S. C., Moldão-Martins, M., Alves, V. D. (2019). Antioxidants of Natural Plant Origins: From Sources to Food Industry Applications. Molecules, 24 (22), 4132. doi: https://doi.org/10.3390/molecules24224132
- Turcov, D., Barna, S., Profire, L., Iacob, A.T., Lisa, G., Puitel, A. C. et al. (2022). Physico-Chemical Characterization of The Antioxidant Mixture Resveratrol-Ferulic Acid for Applications in Dermato-Cosmetic Products. FARMACIA. 70 (3), 410–416. doi: http://doi.org/10.31925/farmacia.2022.3.5
- Sirivibulkovit, K., Nouanthavong, S., Sameenoi, Y. (2018). Paper-based DPPH Assay for Antioxidant Activity Analysis. Analytical Sciences, 34 (7), 795–800. doi: https://doi.org/10.2116/analsci.18p014
- Ivanišová, E., Tokár, M., Mocko, K., Bojňanská, T, Mareček, J., Mendelová, A. (2013). Antioxidant Activity of Selected Plant Products. Journal of Microbiology Biotechnology and Food Sciences, 2 (1), 1692–1703.
- Gurning, K. (2020). Identication of Secondary Metabolic and Test of Activity Ethyl Acetate Fraction of bangun-Bangun (Coleus amboinicus Lour.) Leaves as Antioxidant. Biolink, 7 (1), 117–122. doi: http://doi.org/10.31289/biolink.v7i1.3732
- Khare, R. S., Banerjee, S., Kundu, K. (2011). Coleus Aromaticus Benth-A Nutritive Medicinal Plant of Potential Therapeutic Value. International Journal of Pharma and Bioscience and Technology, 2 (3), 488–500.
- Pillai, P. G., Suresh, P., Aggarwal, G., Doshi, G., Bhatia, V. (2011). Pharmacognostical Standardization and Toxicity Propile of the Methanolic Leaf Extract of Pectranthus amboinicus (Lour) Spreng. Journal of Applied Pharmaceutical Sciences, 1 (2), 75–81.
- Denes, T., Papp, N., Fogarasi, E., Marton, S. E., Varga, E. (2022). Phytochemical Investigation and Antioxidant Potential of Ononis Arvensis L. FARMACIA, 70 (3), 529–535. doi: http://doi.org/ 10.31925/farmacia.2022.3.20
- Gurning, K., Haryadi, W., Sastrohamidjojo, H. (2021). Isolation and Charactericzation of Antioxidant Compounds of Bangun-bangun (Coleus amboinicus, L.) Leaves from North Sumatera, Indonesia. Rasayan Journal Chemistry, 14 (1), 248–253. doi: http://doi.org/10.31788/RJC.2021.1416077
- Sinaga, S. P., Lumbangaol, D. A., Iksen, Situmorang, R. F. R., Gurning, K. (2022). Determination of Phenolic, Flavonoid Content, Antioxidant and Antibacterial Activities of Seri (Muntingia calabura L.) Leaves Ethanol Extract from North Sumatera, Indonesia. Rasayan Journal Chemistry, 15 (2), 1534–1538. doi: http://doi.org/10.31788/RJC.2022.1526730
- William, D.H., Ian, F. (2008). Spectroscopic Methods in Organic Chemistry. London: The Mcbraw-Hill Companies. doi: https://doi.org/10.1055/b-0035-108183
- Žuvela, P., Skoczylas, M., Jay Liu, J., Ba̧czek, T., Kaliszan, R., Wong, M. W., Buszewski, B. (2019). Column Characterization and Selection Systems in Reversed-Phase High-Performance Liquid Chromatography. Chemical Reviews, 119 (6), 3674–3729. doi: https://doi.org/10.1021/acs.chemrev.8b00246
- Jurkaninova, S., Kubinova, R., Nejezchlebova, M., Gazdova, M., Hanakova,Z., Dall’Acqua, S. (2018). Anti-MRSA activity of abietane diterpenes from Coleus blumei Benth. Natural Product Research, 35 (18), 3033–3039. doi: https://doi.org/10.1080/14786419.2019.1686371
- Gaborova, M., Smejkal, K., Kubinova, R. (2022). Abietane Diterpenes of the Genus Plectranthus sensu lato. Molecules, 27 (1), 1–64. doi: https://doi.org/10.3390/molecules27010166
- Garcia, C., Silva, C. O., Monteiro, C. M., Nicolai, M., Viana, A., Andrade, J. M. et al. (2018). Anticancer properties of the abietane diterpene 6,7-dehydroroyleanone obtained by optimized extraction. Future Medicinal Chemistry, 10 (10), 1177–1189. doi: https://doi.org/10.4155/fmc-2017-0239
##submission.downloads##
Опубліковано
Як цитувати
Номер
Розділ
Ліцензія
Авторське право (c) 2022 Kasta Gurning, Winarto Haryadi

Ця робота ліцензується відповідно до Creative Commons Attribution 4.0 International License.
Наше видання використовує положення про авторські права Creative Commons Attribution 4.0 International License для журналів відкритого доступу.
Автори, які публікуються у цьому журналі, погоджуються з наступними умовами:
1. Автори залишають за собою право на авторство своєї роботи та передають журналу право першої публікації цієї роботи на умовах ліцензії Creative Commons Attribution 4.0 International License, котра дозволяє іншим особам вільно розповсюджувати опубліковану роботу з обов'язковим посиланням на авторів оригінальної роботи та першу публікацію роботи у цьому журналі.
2. Автори мають право укладати самостійні додаткові угоди щодо неексклюзивного розповсюдження роботи у тому вигляді, в якому вона була опублікована цим журналом (наприклад, розміщувати роботу в електронному сховищі установи або публікувати у складі монографії), за умови збереження посилання на першу публікацію роботи у цьому журналі.
3. Автори мають право зберігати остаточну прийняту версію статті в інституційному, тематичному або будь-якому іншому репозитарії з метою забезпечення видимості та доступності.







