Дослідження факторів, що впливають на деякі властивості гідрофільних супозиторних основ
DOI:
https://doi.org/10.15587/2519-4852.2023.286315Ключові слова:
супозиторій, основа, розчинник, допоміжна речовина, стійкість до руйнування, час розпадання, вивільнення, абсорбція водиАнотація
Мета. Вивчити вплив складу гідрофільних супозиторних основ на фізико-хімічні та осмотичні властивості виготовлених з них супозиторіїв.
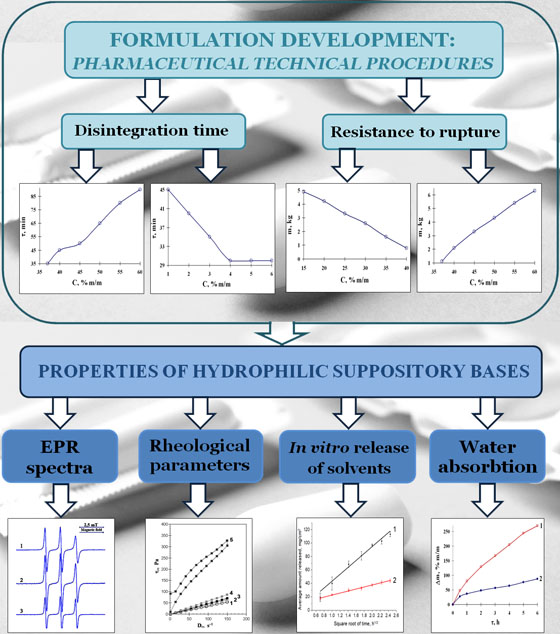
Матеріали та методи. Досліджували основи, в яких варіювали склад допоміжних речовин. Оцінювали мікроструктуру основ, визначали час розпадання та стійкість до руйнування виготовлених з них супозиторіїв. Кінетику абсорбції води та вивільнення розчинників досліджували методом діалізу. Вміст пропіленгліколю (PG) і макроголу 400 (М400) в діалізаті визначали методом газової хроматографії. Розплавлені основи досліджували методом ротаційної віскозиметрії. Отримували спектри електронного парамагнітного резонансу спінових зондів у гідрофільних розчинниках і основах; визначали тип спектра, ізотропну константу (АN), часи кореляції обертальної дифузії (τ), параметр анізотропії (ε).
Результати. Визначено часи розпадання та стійкість супозиторіїв до руйнування залежно від таких факторів, як: вміст та тип полоксамерів, співвідношення між макроголами з високою молекулярною масою і змішаним розчинником PG – М400 (60 : 40 % м/м), співвідношення неіонної ПАР і цетостеарилового спирту (CSA) та їх сумарний вміст, вміст води та твердого жиру. Введення твердого жиру і суміші ПАР з CSA обумовлює рівномірну структуру основ. Значущими факторами, що забезпечують стійкість супозиторіїв до руйнування і прийнятні часи їх розпадання, зменшують абсорбцію води і вивільнення розчинників, є масове співвідношення між ПАР і CSA та їх сумарний вміст. Із зниженням температури з 45 °С до 20 °С основи перетворюються з ньютонівських рідин у тверде тіло. При цьому приблизно в 5 разів зростає в’язкість мікрооточення спінових зондів, але параметри їх обертальної дифузії в твердих основах і змішаному розчиннику PG – M400 є порівнянними. Це свідчить про розчинений стан спінових зондів в основах і відсутність утворення сумісних асоціатів з молекул ПАР і CSA.
Висновки. Варіюючи склад допоміжних речовин можна управляти властивостями гідрофільних супозиторних основ, суттєво знижуючи їх осмотичні властивості. Діючі речовини в цих основах можуть бути в розчиненому стані, що обумовлено високим вмістом неводних розчинників
Посилання
- Buckingham, R. (Ed.) (2020). Martindale: The Complete Drug Reference. London: Pharmaceutical Press, 4912.
- Ul Haq, M. M., Ur Razzak, M. M., Uddin, M. A., Ahmed, N., Shahidulla, S. M. (2021). Rectal Drug Delivery System: An Overview. Clinical Pharmacology and Biopharmaceutics, 10 (5), 219.
- Hua, S. (2019). Physiological and Pharmaceutical Considerations for Rectal Drug Formulations. Frontiers in Pharmacology, 10. doi: https://doi.org/10.3389/fphar.2019.01196
- Melnyk, G., Yarnykh, T., Herasymova, I. (2020). Analytical Review of the Modern Range of Suppository Bases. Systematic Reviews in Pharmacy, 11 (4), 503–508. doi: https://doi.org/10.31838/srp.2020.4.76
- Sheskey, P. J., Hancock, B. C., Moss, G. P., Goldfarb, D. J. (Ed.) (2020). Handbook of Pharmaceutical Excipients. London: Pharm. Press, 1296.
- Szulc-Musiol, B., Bulas, L., Dolinska, B. (2019). Effect of Selected Surfactants on Kinetics of Meloxicam Release from Rectal Suppositories. Indian Journal of Pharmaceutical Sciences, 81 (6), 1115–1121. doi: https://doi.org/10.36468/pharmaceutical-sciences.610
- Ilomuanya, M. O., Ifudu, Ndu. D., Odulaja, J., Igwilo, C. (2012). Assessment of the effect of base type and surfactant on the release properties and kinetics of paracetamol suppositories. Journal of Chemical and Pharmaceutical Research, 4 (6), 3280–3286.
- Kasperek, R., Galczynski, K., Nalesniak, M., Iwaniak, K., Poleszak, E. (2014). Influence of the dissolution medium on the release of dehydroepiandrosterone from lipophilic suppositories. Current Issues in Pharmacy and Medical Sciences, 27 (1), 46–50. doi: https://doi.org/10.2478/cipms-2014-0012
- The European Pharmacopoeia (2022). EDQM. Strasbourg: Council of Europe. Available at: http://pheur.edqm.eu/subhome/11-0
- Hanning, S. M., Matiz, S., Krasser, K., Orlu, M., Dodoo, C., Gaisford, S., Tuleu, C. (2020). Characterisation of rectal amoxicillin (RAMOX) for the treatment of pneumonia in children. Drug Delivery and Translational Research, 11 (3), 944–955. doi: https://doi.org/10.1007/s13346-020-00804-6
- Akhtar, M., Akhtar, N., Ahmad, M., Arif, A. S., Shah, P. A. (2000). Drug release from PEG suppository bases and from their combination with polymers. Journal of Faculty of Pharmacy of Istanbul University, 33, 7–16.
- Zawar, L. R., Bhandari, G. S. (2012). Formulation and Evaluation of Sustained Release Ondansetron Poloxamer Based Solid Suppositories. Journal of Applied Pharmaceutical Science, 2 (7), 186–190. doi: https://doi.org/10.7324/japs.2012.2729
- Havaldar, V. D., Yadav, A. V., Dias, R. J., Mali, K. K., Survase, A. B., Ghorpade, V. S., Salunkhe, N. H. (2017). Screening of Suppository bases for Rectal delivery of Carbamazepine. Research Journal of Pharmacy and Technology, 10 (8), 2697–2703. doi: https://doi.org/10.5958/0974-360x.2017.00479.6
- Ali, M. M., Mashrai A., Al-dholimi, N. (2018). Sustained Release Suppositories of Metoclopramide HCl: Formulation and In vitro Evaluation. Journal of Chemical and Pharmaceutical Research, 10 (1), 169–175.
- Mori, K., Hori, S., Kawata, T., Kogure, S., Matsumoto, K., Hasegawa, T., Akimoto, M. (2017). The in Vitro Release of Indomethacin from Suppositories: Effects of Bases and Comparison of Different Dissolution Methods. Chemical and Pharmaceutical Bulletin, 65 (7), 674–677. doi: https://doi.org/10.1248/cpb.c16-00794
- El Majri, M. A., El Baseir, M. M. (2016). Formulation and evaluation of ibuprofen suppositories. International Research Journal of Pharmacy, 7 (6), 87–90. doi: https://doi.org/10.7897/2230-8407.07670
- Bialik, M., Kuras, M., Sobczak, M., Oledzka, E. (2021). Achievements in Thermosensitive Gelling Systems for Rectal Administration. International Journal of Molecular Sciences, 22 (11), 5500. doi: https://doi.org/10.3390/ijms22115500
- Ban, E., Kim, C.-K. (2013). Design and evaluation of ondansetron liquid suppository for the treatment of emesis. Archives of Pharmacal Research, 36 (5), 586–592. doi: https://doi.org/10.1007/s12272-013-0049-y
- Bodratti, A., Alexandridis, P. (2018). Formulation of Poloxamers for Drug Delivery. Journal of Functional Biomaterials, 9 (1), 11. doi: https://doi.org/10.3390/jfb9010011
- Liapunov, N. A., Bezuglaia, E. P., Fadeikina, A. G., Lysokobylka, A. A., Stolper, Iu. M. (1999). Sozdanie miagkikh lekarstvennykh sredstv na razlichnykh osnovakh. Soobshchenie 1. Issledovanie reologicheskikh svoistv mazei na vodorastvorimykh osnovakh. Farmakom, 6, 10–16.
- Bezugla, O. P., Lyapunov, M. O., Zinchenko, I. O., Lisokobilka, O. A., Liapunova, A. M. (2022). Modeling of processes of solvent diffusion from ointment bases using in vitro experiments. Functional materials, 29 (4), 553–558. doi: https://doi.org/10.15407/fm29.04.553
- Lyapunov, N., Bezuglaya, E., Liapunova, A., Zinchenko, I., Liapunov, O., Lysokobylka, O., Stolper, Y. (2022). Effect of the composition of emulsifiers and the dispersion medium on the properties of bases for semi-solid preparations. ScienceRise: Pharmaceutical Science, 5 (39), 29–45. doi: https://doi.org/10.15587/2519-4852.2022.266001
- Bezuglaya, E., Krasnopyorova, A., Liapunova, A., Zinchenko, I., Lyapunov, N., Sytnik, O. (2023). Influence of physicochemical properties and structure of mixed solvents propylene glycol – macrogol 400 on their in vitro release. ScienceRise: Pharmaceutical Science, 1 (41), 4–13. doi: https://doi.org/10.15587/2519-4852.2023.274468
- Derzhavna Farmakopeia Ukrainy. Druhe vydannia. Vol. 1 (2015). Kharkiv: Derzhavne pidpryiemstvo «Ukrainskyi naukovyi farmakopeinyi tsentr yakosti likarskykh zasobiv», 1128.
- Derzhavna Farmakopeia Ukrainy. Pershe vydannia. Dopovnennia 1 (2004). Kharkiv: Derzhavne pidpryiemstvo «Naukovo-ekspertnyi farmakopeinyi tsentr», 520.
- Draft guideline on quality and equivalence of topical products (2018). CHMP/QWP/708282/2018. Available at: www.ema.europa.eu/en/quality-equivalence-topical-products
- The United States Pharmacopoeia, 41 – NF 36 (2018). The United States Pharmacopoeial Convention. Rockville. Available at: https://www.worldcat.org/title/united-states-pharmacopeia-2018-usp-41-the-national-formulary-nf-36/oclc/1013752699
- Ilić, T., Pantelić, I., Savić, S. (2021). The Implications of Regulatory Framework for Topical Semisolid Drug Products: From Critical Quality and Performance Attributes towards Establishing Bioequivalence. Pharmaceutics, 13 (5), 710. doi: https://doi.org/10.3390/pharmaceutics13050710
- Tiffner, K. I., Kanfer, I., Augustin, T., Raml, R., Raney, S. G., Sinner, F. (2018). A comprehensive approach to qualify and validate the essential parameters of an in vitro release test (IVRT) method for acyclovir cream, 5%. International Journal of Pharmaceutics, 535 (1-2), 217–227. doi: https://doi.org/10.1016/j.ijpharm.2017.09.049
- Bezuglaya, E., Lyapunov, N., Bovtenko, V., Zinchenko, I., Stolper, Y. (2021). Study of pressurised metered dose inhalers for the purpose of standardization of quality attributes characterizing uniformity of dosing. ScienceRise: Pharmaceutical Science, 4 (32), 11–23. doi: https://doi.org/10.15587/2519-4852.2021.238294
- Kuznetcov, A. N. (1976). Metod spinovogo zonda (Osnovy i primenenie). Moscow: Nauka, 210.
- Likhtenshtein, G. I. (1974). Metod spinovykh zondov v molekuliarnoi biologii. Moscow: Nauka, 256.
##submission.downloads##
Опубліковано
Як цитувати
Номер
Розділ
Ліцензія
Авторське право (c) 2023 Elena Bezuglaya, Yurij Stolper, Nikolay Lyapunov, Igor Zinchenko, Oleksii Liapunov

Ця робота ліцензується відповідно до Creative Commons Attribution 4.0 International License.
Наше видання використовує положення про авторські права Creative Commons Attribution 4.0 International License для журналів відкритого доступу.
Автори, які публікуються у цьому журналі, погоджуються з наступними умовами:
1. Автори залишають за собою право на авторство своєї роботи та передають журналу право першої публікації цієї роботи на умовах ліцензії Creative Commons Attribution 4.0 International License, котра дозволяє іншим особам вільно розповсюджувати опубліковану роботу з обов'язковим посиланням на авторів оригінальної роботи та першу публікацію роботи у цьому журналі.
2. Автори мають право укладати самостійні додаткові угоди щодо неексклюзивного розповсюдження роботи у тому вигляді, в якому вона була опублікована цим журналом (наприклад, розміщувати роботу в електронному сховищі установи або публікувати у складі монографії), за умови збереження посилання на першу публікацію роботи у цьому журналі.
3. Автори мають право зберігати остаточну прийняту версію статті в інституційному, тематичному або будь-якому іншому репозитарії з метою забезпечення видимості та доступності.







