Фармацевтичне забезпечення лікування епілепсії у дітей в Україні та за кордоном
DOI:
https://doi.org/10.15587/2519-4852.2023.286425Ключові слова:
епілепсія, протиепілептичні лікарські засоби, фармацевтичне забезпечення, протоколи лікування, реєстрація, економічна доступність, національний фармацевтичний ринок, маркетинговий аналізАнотація
Мета: дослідити фармацевтичне забезпечення лікування епілепсії у дітей в Україні й за кордоном та провести маркетинговий аналіз українського ринку протиепілептичних лікарських засобів (ЛЗ).
Матеріали та методи: об’єктами дослідження стали українські й зарубіжні інтернет-джерела, медико-технологічні документи за визначеною темою дослідження, нормативно-правова база України, матеріали Державного формуляру, Державний реєстр ЛЗ України. Були використані методи маркетингового аналізу, графічний, документального і аналітичного узагальнення.
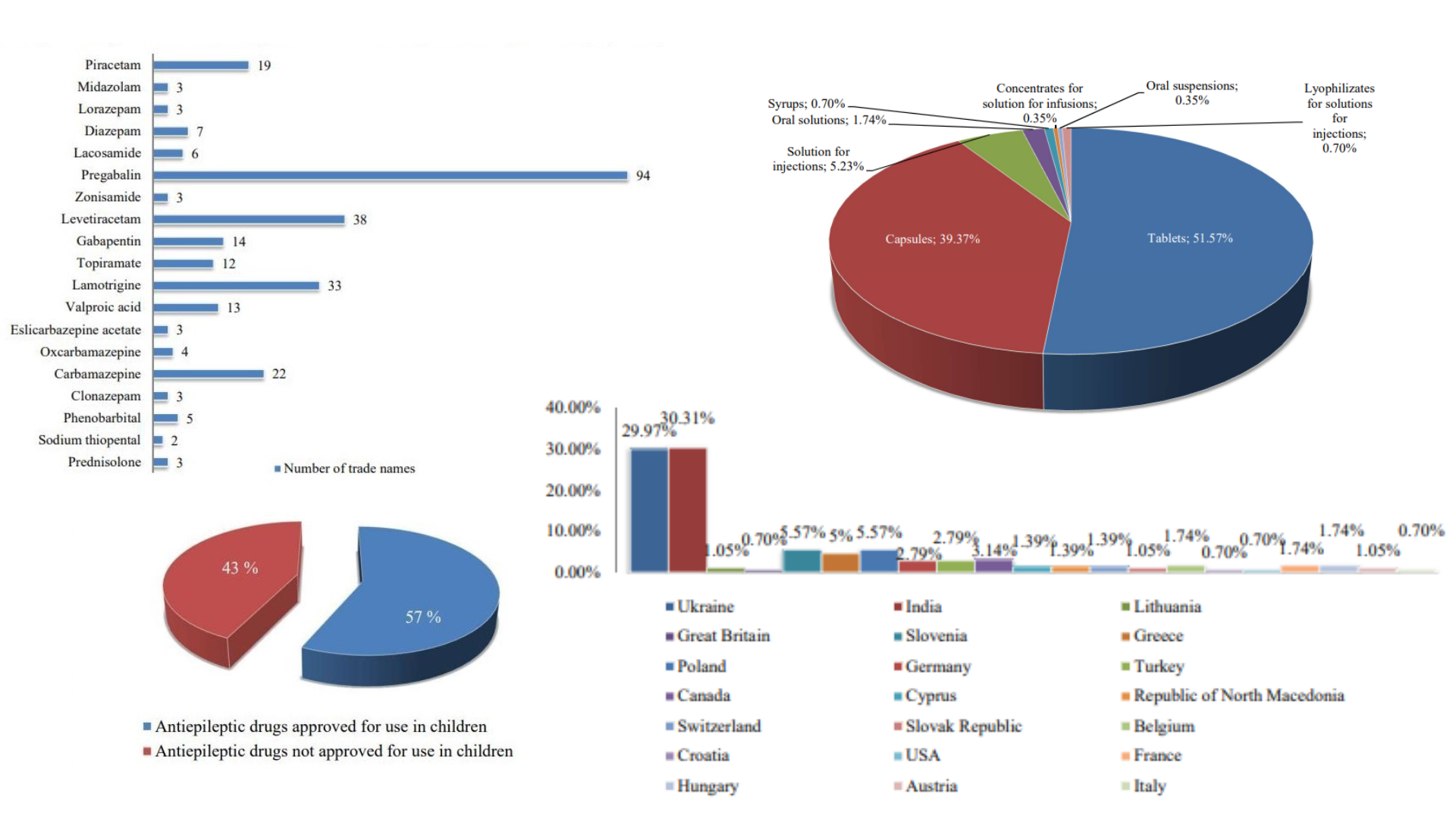
Результати: порівняльний аналіз протоколів (Франція, Великобританія та Україна) лікування епілепсії у дітей показав, що з 37 міжнародних непатентованих назв (МНН) доступних у Франції та Великобританії в Україні доступними (дозволеними) є лише 12 МНН. Аналіз формулярних переліків ЛЗ Великої Британії (БНФД) та України показав, що БНФД налічує 32 МНН, а український – 10 МНН. Станом на жовтень 2022 року в Україні зареєстровано 287 найменувань протиепілептичних ЛЗ і з них 164 ЛЗ дозволені у дитячій практиці. Основними виробниками протиепілептичних ЛЗ є Індія та Україна. Дитячі лікарські форми представлені переважно таблетками та капсулами – більше 90%. У ході порівняння переліків ЛЗ для лікування епілепсії з Національного переліку основних ЛЗ України, БНФД, Примірного переліку ЛЗ ВООЗ та Примірного переліку ВООЗ для дітей було встановлено, що з 37 МНН доступних на міжнародному фармацевтичному ринку спільними для усіх переліків є 11 МНН ЛЗ, що наявні у всіх документах.
Висновки: Результати комплексного дослідження свідчать про необхідність покращення фармацевтичного забезпечення лікування епілепсії в Україні, порівняно з закордонною практикою. Зарубіжні протоколи лікування включають ЛЗ на основі високоочищеного канабісу, які реімбурсуються (Велика Британія), та дозволені до використання у Європейському Союзі, але національна нормативно-правова база не дозволяє використання цих ЛЗ, що вказує на необхідність внесення змін до законодавчої бази України. Доцільним буде розширення номенклатури та лікарських форм для дитячої практики, що забезпечить підвищення прихильності пацієнта до лікування та дозволить підвищити ефективність фармакотерапії
Посилання
- Epilepsy (2023). Available at: https://www.who.int/news-room/fact-sheets/detail/epilepsy
- Panayiotopoulos C.P. (2010). Epileptic Syndromes and their Treatment. London: Springer¬Verag, 620.
- Shcho treba znaty pro epilepsiiu (2019). Available at: https://www.phc.org.ua/news/scho-treba-znati-pro-epilepsiyu
- Polozhennia pro unifikovanyi klinichnyi protokol pervynnoi, ekstrenoi, vtorynnoi (spetsializovanoi) ta tretynnoi (vysokospetsializovanoi) medychnoi dopomohy "Epilepsii u ditei" (2014). Nakaz MOZ Ukrainy No. 276 v0276282-14. 17.04.2014. Available at: zakon.rada.gov.ua/rada/show/v0276282-14#Text
- Kozolkin, O. A., Vizir, I. V., Sikorska, M. V. (2019). Epilepsiia. Suchasni pryntsypy diahnostyky i likuvannia. Zaporizhzhia: ZDMU, 153. Available at: http://dspace.zsmu.edu.ua/handle/123456789/12135
- Who We Are. European Academy of Neurology. Available at: https://www.ean.org/home/about-us/who-we-are
- About the American Neurological Association (2022). American Neurological Association. Available at: https://myana.org/about-american-neurological-association
- British Paediatric Neurology Association. Available at: bpna.org.uk/
- Epilepsy Foundation. Available at: epilepsy.com/about-us/about-foundation
- Association Epilepsie-France. Available at: http://www.epilepsie-france.com/notre-association/qui-sommes-nous.html
- International League Against Epilepsy. Available at: https://www.ilae.org/
- Épilepsies: Prise en charge des enfants et des adultes. Recommandation. Available at: has-sante.fr/upload/docs/application/pdf/2020-10/reco308_recommandations_epilepsies_preparation_mel.pdf
- Epilepsies in children, young people and adults. NICE guideline [NG217] (2022). Available at: https://www.nice.org.uk/guidance/NG217
- British National Formulary for Children 2019–2020. Available at: https://nhathuocngocanh.com/wp-content/uploads/pdf/BNFC-2019-2020.pdf
- Unifikovanyi klinichnyi protokol pervynnoi, ekstrenoi, vtorynnoi (spetsializovanoi) ta tretynnoi (vysokospetsializovanoi) medychnoi dopomohy "Epilepsii u ditei". Available at: https://www.dec.gov.ua/wp-content/uploads/2019/11/2014_276_ykpmd_epilepsiya_dity.pdf
- Pro zatverdzhennia chotyrnadtsiatoho vypusku Derzhavnoho formuliara likarskykh zasobiv ta zabezpechennia yoho dostupnosti (2022). Nakaz MOZ Ukrainy No. 1011. 13.06.2022. Available at: https://moz.gov.ua/article/ministry-mandates/nakaz-moz-ukraini-vid-13062022--1011-pro-zatverdzhennja-chotirnadcjatogo-vipusku-derzhavnogo-formuljara-likarskih-zasobiv-ta-zabezpechennja-jogo-dostupnosti
- Epidyolex (cannabidiol). An overview of Epidyolex and why it is authorised in the EU. EMA/191061/2021. Available at: https://www.ema.europa.eu/en/documents/overview/epidyolex-epar-medicine-overview_en.pdf
- Burns, C. (2019). NICE recommends first cannabis-based medicines for use on the NHS. The Pharmaceutical Journal, 303 (7931). doi: https://doi.org/10.1211/pj.2019.20207320
- Aliekperova, N., Kosyachenko, K., Kaniura, O. (2020). Perspectives on formation of medical cannabis market in Ukraine based on holistic approach. Journal of Cannabis Research, 2 (1). doi: https://doi.org/10.1186/s42238-020-00044-y
- Alekperova, N. V. (2019). Analysis of drugs that are used in the cannabis market for medical purposes. Retsept, 22 (6), 938–945.
- Sholoiko, N. V., Popov, V. I., Lysenko, T. I. (2019). Suchasnyi stan ta perspektyvy zastosuvannia konopel u medytsyni ta farmatsii (Ohliad literatury). Fitoterapiia. Chasopys, 1, 44–52.
- Pro vnesennia zmin do nakazu Ministerstva okhorony zdorov’ia Ukrainy vid 28 veresnia 2012 roku № 751 (2016). Nakaz MOZ Ukrainy No. 1422 z0530-17. 29.12.2016. Available at: https://zakon.rada.gov.ua/laws/show/z0530-17#Text
- Polozhennia pro Derzhavnyi reiestr likarskykh zasobiv (2004). Postanova Kabinetu Ministriv Ukrainy No. 411. 31.03.2004. Available at: https://zakon.rada.gov.ua/laws/show/411-2004-%D0%BF#Text
- "Derzhavnyi reiestr likarskykh zasobiv Ukrainy" Informatsiinyi fond. Available at: http://www.drlz.com.ua/
- Perucca, E. (2002). Pharmakological and therapeutic properties of valproate. A summary after 35 year of clinical experience. CNS Drugs, 16 (10), 695–714. doi: https://doi.org/10.2165/00023210-200216100-00004
- Hirsch, L. J., Weintraub, D. B., Buchsbaum, R., Spencer, H. T., Straka, T., Hager, M., Resor, S. R. (2006). Predictors of Lamotrigine-associated Rash. Epilepsia, 47 (2), 318–322. doi: https://doi.org/10.1111/j.1528-1167.2006.00423.x
- Teresk, M. G., Berkland, C. J., Dormer, N. H. (2017). Deficiencies in Traditional Oral Dosage Forms and the Emergence of Controlled-Release Powder Manufacturing. KONA Powder and Particle Journal, 34, 91–105. doi: https://doi.org/10.14356/kona.2017013
- Kale, R. (2002). The Treatment Gap. Epilepsia, 43, 31–33. doi: https://doi.org/10.1046/j.1528-1157.43.s.6.13.x
- Horachuk, V. V. (2011). Medical, social and economic aspects of epilepsy. Ukrainskyi medychnyi chasopys, 5 (85), 9–10. Available at: https://www.umj.com.ua/article/18382/mediko-socialni-ta-ekonomichni-aspekti-epilepsii
- Vitchyzniana epileptolohiia: profesiini dosiahnennia ta mizhnarodne vyznannia (2021). NeiroNews: psykhonevrolohiia ta neiropsykhiatriia, 1 (122). Available at: https://neuronews.com.ua/ua/archive/2021/1%28122%29/pages-11-15/vitchiznyana-epileptologiya-profesiyni-dosyagnennya-ta-mizhnarodne-viznannya#gsc.tab=0
- World Health Organization model list of essential medicines: 21st list 2019 (2019). Geneva, 2019. Available at: https://www.who.int/publications/i/item/WHOMVPEMPIAU2019.06
- Shaw, B. (2019). The WHO’s Essential Medicines List: Changing the Conversation. Available at: https://pharmaboardroom.com/articles/the-whos-essential-medicines-list-changing-the-conversation/
- Pro likarski zasoby (1996). Zakon Ukrainy No. 123/96-VR. 04.04.1996. Available at: https://zakon.rada.gov.ua/laws/show/123/96-%D0%B2%D1%80#Text
- Osnovy zakonodavstva Ukrainy pro okhoronu zdorov’ia (1993). Zakon Ukrainy No. 2801-XII. 19.11.1992. Available at: https://zakon.rada.gov.ua/laws/show/2801-12#Text
- Dostupni liky. Available at: https://moz.gov.ua/dostupni-liki
- Yak pratsiuie prohrama reimbursatsii «Dostupni liky» z onovlenym reiestrom likarskykh zasobiv (2023). Available at: https://medplatforma.com.ua/article/1975-yak-pratsyu-programa-rembursats-dostupn-lki-z-1-jovtnya
- World Health Organization Model List of Essential Medicines for Children (2021). Geneva: World Health Organization. Available at: https://www.who.int/publications/i/item/WHO-MHP-HPS-EML-2021.03
- Pro derzhavni finansovi harantii medychnoho obsluhovuvannia naselennia (2017). Zakon Ukrainy No. 2168-VIII. 19.10.2017. Available at: https://zakon.rada.gov.ua/laws/show/2168-19#Text
- Gonchar, A., Sholoiko, N. (2022). Consumption analysis of two-component fixed combinations of medicines for arterial hypertension treatment in Ukraine as one of the stages for evaluation of their reimbursement prospects. ScienceRise: Pharmaceutical Science, 4 (38), 19–27. doi: https://doi.org/10.15587/2519-4852.2022.263733
- Fedotova, M., Panfilova, H., Hala, L., Lebedyn, A., Simonian, L., Gerush, O. et al. (2022). Evaluation of the state of pharmaceutical supply of patients with dementia with Alzheimer disease in Ukraine in accordance with international recommendations. ScienceRise: Pharmaceutical Science, 4 (38), 53–61. doi: https://doi.org/10.15587/2519-4852.2022.263415
- Kostiuk, I. A. (2019). Analysis of dynamics of the medcine list in the government program «available medicines» for treatment of bronchial asthma. Farmatsevtychnyi Zhurnal, 5 (74), 12–20. doi: https://doi.org/10.32352/0367-3057.5.19.02
- Vlasenko, I. O., Davtian, L. L. (2021). Pharmaceutical provision of insulin in Ukraine 2016–2021. Pharmaceutical Review, 2, 55–64. doi: https://doi.org/10.11603/2312-0967.2021.2.12176
- Hrynkiv, Ya. O., Blavatska, O. B., Lozynska, M. O. (2015). Information-organizational providing of pharmaceutical care for patients with epilepsy. Pharmaceutical Review, 2, 68–71. Available at: http://nbuv.gov.ua/UJRN/Phch_2015_2_15
##submission.downloads##
Опубліковано
Як цитувати
Номер
Розділ
Ліцензія
Авторське право (c) 2023 Natalia Sholoiko, Liliia Hala, Kostyantyn Kosyachenko, Myroslava Hubar

Ця робота ліцензується відповідно до Creative Commons Attribution 4.0 International License.
Наше видання використовує положення про авторські права Creative Commons Attribution 4.0 International License для журналів відкритого доступу.
Автори, які публікуються у цьому журналі, погоджуються з наступними умовами:
1. Автори залишають за собою право на авторство своєї роботи та передають журналу право першої публікації цієї роботи на умовах ліцензії Creative Commons Attribution 4.0 International License, котра дозволяє іншим особам вільно розповсюджувати опубліковану роботу з обов'язковим посиланням на авторів оригінальної роботи та першу публікацію роботи у цьому журналі.
2. Автори мають право укладати самостійні додаткові угоди щодо неексклюзивного розповсюдження роботи у тому вигляді, в якому вона була опублікована цим журналом (наприклад, розміщувати роботу в електронному сховищі установи або публікувати у складі монографії), за умови збереження посилання на першу публікацію роботи у цьому журналі.
3. Автори мають право зберігати остаточну прийняту версію статті в інституційному, тематичному або будь-якому іншому репозитарії з метою забезпечення видимості та доступності.







