Розробка та характеристика наночастинок езетимібу для лікування гіперліпідемії
DOI:
https://doi.org/10.15587/2519-4852.2026.359581Ключові слова:
Езетиміб, ВЕРХ, альгінат натрію, наночастинкиАнотація
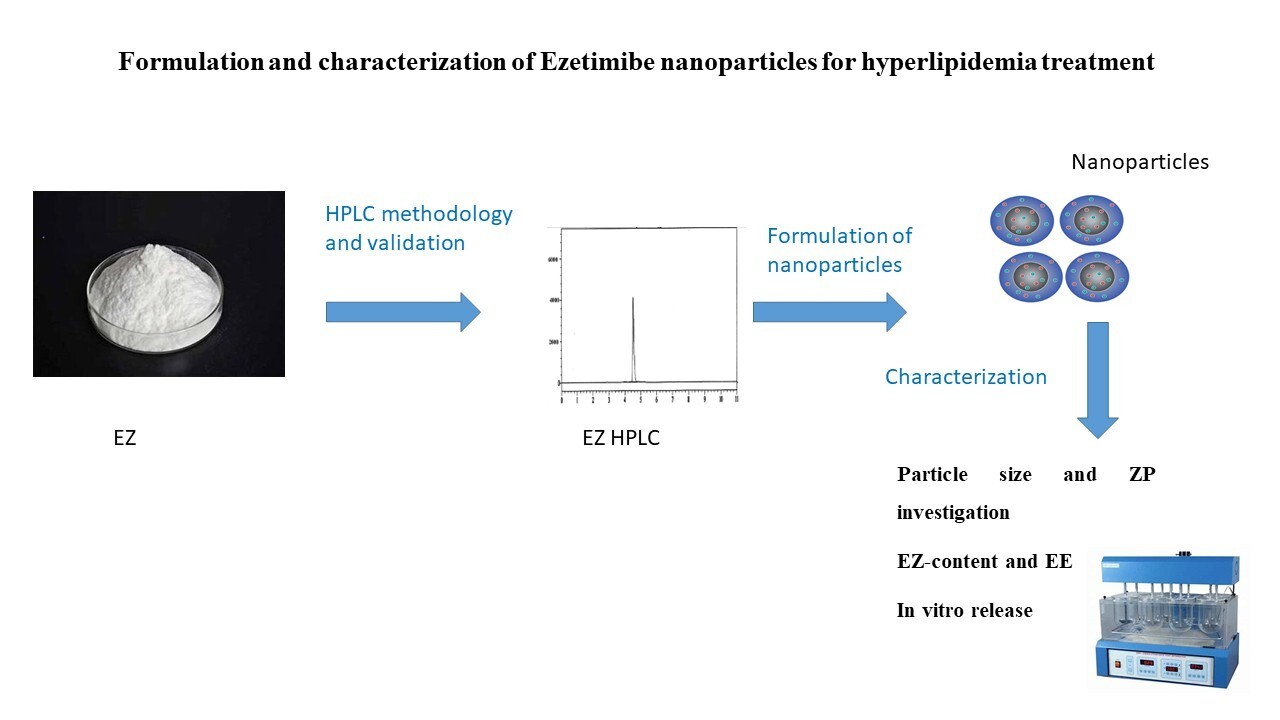
Мета роботи. Езетиміб належить до лікарських засобів II класу за Біофармацевтичною класифікаційною системою (BCS II), що характеризуються низькою розчинністю та високою проникністю. Метою цієї роботи було інкорпорувати езетиміб у наночастинки для прискорення вивільнення та підвищення його біодоступності.
Матеріали та методи. Було розроблено стабільність-індикативний метод для кількісного визначення езетимібу у наночастинках у свіжоприготованих та збережених зразках. Дев’ять варіацій наночастинок езетимібу було отримано методом випаровування розчинника з використанням ГПМЦ 6 cps, альгінату натрію та Твін 80 у різних співвідношеннях. Для визначення вмісту езетимібу у наночастинках було розроблено метод ВЕРХ. Наночастинки езетимібу були досліджені хімічно та охарактеризовані.
Результати. Розроблений метод був повністю валідований, а наночастинки езетимібу, що містили ГПМЦ і Твін 80, мали дзета-потенціал у межах від –21,6 мВ до –30,1 мВ, що було вищим порівняно з іншими складами, і характеризувалися покращеним вивільненням. Склад (HP4) мав найвищий дзета-потенціал (–30,1 мВ) і забезпечував вивільнення близько 91% езетимібу протягом 20 хв. Саме HP4 було обрано для оцінки стабільності, за результатами якої її було підтверджено.
Висновки. Склад (HP4), що містив співвідношення езетиміб:ГПМЦ:альгінат натрію 0,1:0,5:0,4, була оптимізованою формою наночастинок езетимібу. Мікроінкапсуляція езетимібу з ГПМЦ та альгінатом натрію у співвідношенні 0,1:0,5:0,4 сприяла підвищенню вивільнення та забезпеченню стабільності
Посилання
- Nițu, E.-T., Jianu, N., Merlan, C., Foica, D., Sbârcea, L., Buda, V. et al. (2025). A Comprehensive Review of the Latest Approaches to Managing Hypercholesterolemia: A Comparative Analysis of Conventional and Novel Treatments: Part I. Life, 15 (8), 1185. https://doi.org/10.3390/life15081185
- Kumari, L., Rani, D. (2025). A Concise overview of diverse analytical techniques for ezetimibe estimation. Microchemical Journal, 209, 112561. https://doi.org/10.1016/j.microc.2024.112561
- Torrado-Salmerón, C., Guarnizo-Herrero, V., Gallego-Arranz, T., del Val-Sabugo, Y., Torrado, G., Morales, J., Torrado-Santiago, S. (2020). Improvement in the Oral Bioavailability and Efficacy of New Ezetimibe Formulations – Comparative Study of a Solid Dispersion and Different Micellar Systems. Pharmaceutics, 12 (7), 617. https://doi.org/10.3390/pharmaceutics12070617
- Lipinski, C. A. (2000). Drug-like properties and the causes of poor solubility and poor permeability. Journal of Pharmacological and Toxicological Methods, 44 (1), 235–249. https://doi.org/10.1016/s1056-8719(00)00107-6
- Zhuo, Y., Zhao, Y.-G., Zhang, Y. (2024). Enhancing Drug Solubility, Bioavailability, and Targeted Therapeutic Applications through Magnetic Nanoparticles. Molecules, 29 (20), 4854. https://doi.org/10.3390/molecules29204854
- A. Ali, Y., N. Abd-Alhammid, S. (2017). Formulation and Evaluation of Ezetimibe Nanoparticles. Iraqi Journal of Pharmaceutical Sciences, 24 (2), 11–21. https://doi.org/10.31351/vol24iss2pp11-21
- Q 2 (R1) Validation of Analytical Procedures: Text and Methodology (1995). European Medicines Agency. Available at: https://www.ema.europa.eu/en/documents/scientific-guideline/ich-guideline-q2r1-validation-analytical-procedures-text-methodology-step-5-first-version_en.pdf
- The Pharmacopoeia of United States of America (2020). National Formulary 38, Mack publishing Co. Easton, vol. 2. Available at: http://182.160.97.198:8080/xmlui/handle/123456789/1493
- Singh, R., Popli, H., Suryawanshi, M. (2025). Development and validation of an HPLC analytical method for the simultaneous estimation of vitamin B12 and folic acid. Essential Chem, 2 (1), 1–9. https://doi.org/10.1080/28378083.2025.2462931
- Rostami, E. (2021). Recent achievements in sodium alginate-based nanoparticles for targeted drug delivery. Polymer Bulletin, 79 (9), 6885–6904. https://doi.org/10.1007/s00289-021-03781-z
- Filimon, A., Onofrei, M. D., Bargan, A., Stoica, I., Dunca, S. (2023). Bioactive Materials Based on Hydroxypropyl Methylcellulose and Silver Nanoparticles: Structural-Morphological Characterization and Antimicrobial Testing. Polymers, 15 (7), 1625. https://doi.org/10.3390/polym15071625
- Li, H.-J., Zhang, A.-Q., Hu, Y., Sui, L., Qian, D.-J., Chen, M. (2012). Large-scale synthesis and self-organization of silver nanoparticles with Tween 80 as a reductant and stabilizer. Nanoscale Research Letters, 7 (1). https://doi.org/10.1186/1556-276x-7-612
- Elhassan, E., Omolo, C. A., Gafar, M. A., Ismail, E. A., Ibrahim, U. H., Khan, R. et al. (2025). Multifunctional hyaluronic acid-based biomimetic/pH-responsive hybrid nanostructured lipid carriers for treating bacterial sepsis. Journal of Biomedical Science, 32 (1). https://doi.org/10.1186/s12929-024-01114-6
- Jafar, M., Sajjad Ahmad Khan, M., Salahuddin, M., Zahoor, S., MohammedHesham Slais, H., Ibrahim Alalwan, L., Radhi Alshaban, H. (2023). Development of apigenin loaded gastroretentive microsponge for the targeting of Helicobacter pylori. Saudi Pharmaceutical Journal, 31 (5), 659–668. https://doi.org/10.1016/j.jsps.2023.03.006
- Castro, S. R., Ribeiro, L. N. M., Breitkreitz, M. C., Guilherme, V. A., Rodrigues da Silva, G. H., Mitsutake, H. et al. (2021). A pre-formulation study of tetracaine loaded in optimized nanostructured lipid carriers. Scientific Reports, 11 (1). https://doi.org/10.1038/s41598-021-99743-6
- Dissolution Methods. FDA. Available at: https://www.accessdata.fda.gov/scripts/cder/dissolution/dsp_SearchResults.cfm
- Rahi, F. A., Mohammed Ameen, M. S., Fayyadh, M. S. (2021). Linagliptin and gliclazide di-loaded extended-release nanoparticles: formulation and evaluation. Wiadomości Lekarskie, 74 (9), 2315–2322. https://doi.org/10.36740/wlek202109212
- Rahi, F. A., Ameen, M. S. M., Jawad, K. K. M. (2022). Preparation and evaluation of lipid matrix microencapsulation for drug delivery of azilsartan kamedoxomil. ScienceRise: Pharmaceutical Science, 6 (40), 21–28. https://doi.org/10.15587/2519-4852.2022.270306
- Singh, N., Akhtar, M. J., Anchliya, A. (2021). Development and Validation of HPLC Method for Simultaneous Estimation of Reduced and Oxidized Glutathione in Bulk Pharmaceutical Formulation. Austin Journal of Analytical and Pharmaceutical Chemistry, 8 (1). https://doi.org/10.26420/austininternmed.2021.1129
- Sudha, T., Sumithra, M., Ajith, U. (2024). A review of analytical method development and validation of labetalol hydrochloride. Annals of Phytomedicine an International Journal, 13 (1). https://doi.org/10.54085/ap.2024.13.1.38
- Mahapatra, A., Sreedhar, C. (2018). HPLC and analytical method validation: a review. Indian Research Journal of Pharmacy and Science, 5 (1), 1399–1414. https://doi.org/10.21276/irjps.2018.5.1.18
- Nakatuka, Y., Yoshida, H., Fukui, K., Matuzawa, M. (2015). The effect of particle size distribution on effective zeta-potential by use of the sedimentation method. Advanced Powder Technology, 26 (2), 650–656. https://doi.org/10.1016/j.apt.2015.01.017
- Elkhayat, D., Abdelmalak, N. S., Amer, R., Awad, H. H. (2025). Ezetimibe Loaded Nanostructured Lipid Carriers Tablets: Response Surface Methodology, In-vitro Characterization, and Pharmacokinetics Study in Rats. Journal of Pharmaceutical Innovation, 20 (1). https://doi.org/10.1007/s12247-024-09911-0
- Tulain, U. R., Mahmood, A., Aslam, S., Erum, A., Shamshad Malik, N., Rashid, A. et al. (2021). Formulation and Evaluation of Linum usitatissimum Mucilage-Based Nanoparticles for Effective Delivery of Ezetimibe. International Journal of Nanomedicine, 16, 4579–4596. https://doi.org/10.2147/ijn.s308790
##submission.downloads##
Опубліковано
Як цитувати
Номер
Розділ
Ліцензія
Авторське право (c) 2026 Asmaa Abdelaziz Mohamed, Olla Maan, Firas Aziz Rahi, Doaa Zakaria Elkashif

Ця робота ліцензується відповідно до Creative Commons Attribution 4.0 International License.
Наше видання використовує положення про авторські права Creative Commons Attribution 4.0 International License для журналів відкритого доступу.
Автори, які публікуються у цьому журналі, погоджуються з наступними умовами:
1. Автори залишають за собою право на авторство своєї роботи та передають журналу право першої публікації цієї роботи на умовах ліцензії Creative Commons Attribution 4.0 International License, котра дозволяє іншим особам вільно розповсюджувати опубліковану роботу з обов'язковим посиланням на авторів оригінальної роботи та першу публікацію роботи у цьому журналі.
2. Автори мають право укладати самостійні додаткові угоди щодо неексклюзивного розповсюдження роботи у тому вигляді, в якому вона була опублікована цим журналом (наприклад, розміщувати роботу в електронному сховищі установи або публікувати у складі монографії), за умови збереження посилання на першу публікацію роботи у цьому журналі.
3. Автори мають право зберігати остаточну прийняту версію статті в інституційному, тематичному або будь-якому іншому репозитарії з метою забезпечення видимості та доступності.







