Дві майстерні альтернативні спектрофотометричні методики визначення раміприлу в таблетках
DOI:
https://doi.org/10.15587/2519-4852.2024.302635Ключові слова:
раміприл, спектрофотометрія, валідація, кількісне визначення, таблеткиАнотація
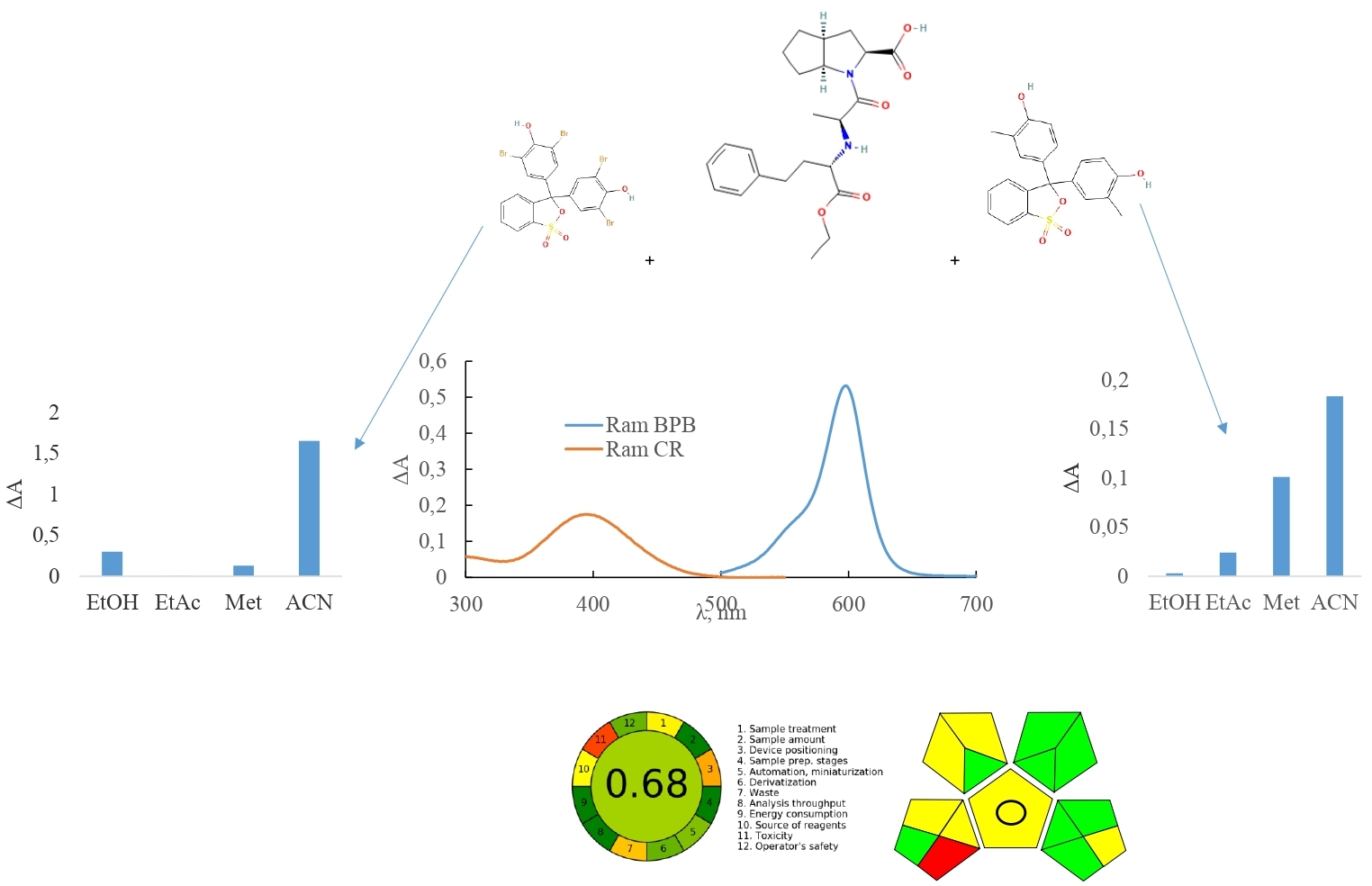
Метою роботи була розробка двох простих, економічно доступних, альтернативних спектрофотометричних методик визначення раміприлу в таблетках на основі реакції з сульфофталеїновими барвниками (бромфеноловим синім (BPB) та крезоловим червоним (CR)).Матеріали та методи. Аналітичне обладнання: двопроменевий спектрофотометр Shimadzu UV-1800 (Японія) з програмним забезпеченням UV-Probe 2.62, ваги аналітичні RAD WAG AS 200/C (Польща). Раміприл (чистота ≥98 % (ВЕРХ)) був придбаний у AARTI Industries Limited (Індія). Таблетки Раміприл 5 мг, 10 мг були придбані в місцевій аптеці.Результати та обговорення. Розроблено дві спектрофотометричні методики визначення раміприлу в таблетках. Нами були протестовані різні сульфофталеїнові барвники (BPB, бромкрезоловий зелений, бромтимоловий синій, тимоловий синій, CR) з метою вибору оптимального для розробки методики. За результатами експериментальних досліджень в якості реактивів ми обрали BPB і CR, а розчинником для обох методик був ацетонітрил. Встановлено оптимальні умови для кількісного визначення раміприлу в таблетках за допомогою BPB: концентрація – 2,35×10-4 моль/л, об’єм розчину BPB – 1,0 мл, без нагрівання, довжина хвилі – 598 нм, час реакції – 5 хв, температура розчину – 25 °С. Встановлено оптимальні умови для кількісного визначення раміприлу в таблетках за допомогою CR: концентрація – 1,33×10-4 моль/л, об’єм розчину CR – 1,0 мл, без нагрівання, довжина хвилі – 395 нм, час реакції – 5 хв, температура розчину – 25 °С. Спектрофотометрична методика з використанням BPB була лінійною в діапазоні концентрацій 1,99-5,96 мкг/мл, МВ – 0,20 мкг/мл, МКВ – 0,60 мкг/мл. Спектрофотометрична методика із застосуванням CR була лінійною в діапазоні концентрацій 0,42-5,44 мкг/мл, МВ – 0,10 мкг/мл, МКВ – 0,36 мкг/мл. Результати дослідження робасності, правильності та прецизійності відповідали критеріям прийнятності. Результати дослідження «зеленості» обох методик свідчать про відмінний «зелений» аналіз.Висновки. Розроблені методики можуть бути використані як альтернативні для рутинного аналізу таблеток раміприлу
Посилання
- Cardiovascular Diseases (CVDs). Available at: https://www.who.int/health-topics/cardiovascular-diseases#tab=tab_3 Last accessed: 22.03.2024
- Ramipril. Available at: https://pubchem.ncbi.nlm.nih.gov/compound/Ramipril Last accessed: 14.03.2024
- European Pharmacopoeia. 11 ed. (2022). Available at: https://www.edqm.eu/en/european-pharmacopoeia-ph.-eur.-11th-edition Last accessed: 22.03.2024
- Babu, K. A., Kumar, G. V., Sivasubramanian, L. (2011). Simultaneous estimation of ramipril and amlodipine in pharmaceutical dosage form by RP-HPLC method. International Journal of Pharmacy and Pharmaceutical Sciences, 3 (4), 196–198.
- Dai, S.-Y., Qiu, S.-T., Wu, W., Fu, C.-M. (2013). Development and validation of an RP-HPLC method for simultaneous determination of Ramipril and Amlodipine in tablets. Journal of Pharmaceutical Analysis, 3 (6), 440–446. https://doi.org/10.1016/j.jpha.2013.09.002
- Elshanawane, A. A., Mostafa, S. M., Elgawish, M. S. (2008). Application of a Validated, Stability-Indicating LC Method to Stress Degradation Studies of Ramipril and Moexipril.HCl. Chromatographia, 67 (7-8), 567–573. https://doi.org/10.1365/s10337-008-0544-3
- Gupta, K. R., Wankhede, S. B., Tajne, M. R., Wadodkar, S. G. (2007). Simultaneous determination of amlodipine and ramipril by high performance thin layer chromatography. Asian Journal of Chemistry, 19 (6), 4177–4182.
- Kumar, P. V., Nasare, M., Rao, V., Prasad, V. V. L. N., Diwan, P. V. (2012). Isocratic Reverse Phase High Performance Liquid Chromatographic Estimation of Ramipril and Amlodipine in Pharmaceutical Dosage Form. Journal of Advanced Pharmacy Education and Research, 2 (3), 137–145.
- Maste, M. M., Kalekar, M. C., Kadian, N., & Bhat, A. R. (2011). Development of RP-HPLC Method for Simultaneous Estimation of Amlodipine and Ramipril in Tablet Dosage form. Asian Journal of Research in Chemistry, 4(8), 1210-1213.
- Panchal, H. J., Suhagia, B. N., Patel, N. J., Rathod, I. S., Patel, B. H. (2008). Simultaneous Estimation of Atorvastatin Calcium, Ramipril and Aspirin in Capsule Dosage Form by RP-LC. Chromatographia, 69 (1-2), 91–95. https://doi.org/10.1365/s10337-008-0831-z
- Patel, J., Patel, M. (2014). RP-HPLC method development and validation for the simultaneous estimation of ramipril and amlodipine besylate in capsule dosage form. Journal of Chemical and Pharmaceutical Research, 6 (6), 725–733.
- Damle, M. S., Patole, S. M., Potale, L. V., Khodke, A. S. (2010). A validated HPLC method for analysis of atorvastatin calcium, ramipril and aspirin as the bulk drug and in combined capsule dosage Forms. International Journal of Pharmaceutical Sciences Review and Research, 4 (3), 40–45.
- Rajput, P. S., Kaur, A., Gill, N. K., Mittal, K., Sarma, G. S. (2012). Simultaneous estimation of ramipril and amlodipine in bulk and tablet dosage form by RP-HPLC method. Journal of Applied Pharmaceutical Science, 2 (7), 160–165. https://doi.org/10.7324/japs.2012.2724
- Dheeravath, S. N., Ramadevi, K., Saraswathi, Z., Maniklal, D., Bhagawan. D, Bhagawan. D. (2012). RP-HPLC method development for simultaneous determination of the drugs Ramipril and Amlodipine. International Journal of Scientific Research, 2 (2), 364–367. https://doi.org/10.15373/22778179/feb2013/123
- Sharma, R., Khanna, S., Mishra, G. P. (2012). Development and Validation of RP-HPLC Method for Simultaneous Estimation of Ramipril, Aspirin and Atorvastatin in Pharmaceutical Preparations. E-Journal of Chemistry, 9 (4), 2177–2184. https://doi.org/10.1155/2012/891695
- Rao, S., Srinivas, K. (2010). RP-HPLC method for the determination of losartan potassium and ramipril in combined dosage form. Indian Journal of Pharmaceutical Sciences, 72 (1), 108–111. https://doi.org/10.4103/0250-474x.62243
- Joseph, L., Mathew, G., Rao, V. R. (2008). Simultaneous estimation of atorvastatin and ramipril by RP-HPLC and spectroscopy. Pakistan journal of pharmaceutical sciences, 21 (3), 282–284.
- Sharma, A. K., Shah, B., Patel, B. (2010). Simultaneous estimation of Atorvastatin calcium, Ramipril and Aspirin in capsule dosage form using HPTLC. Der Pharma Chemica, 2 (4), 10–16.
- Żuromska-Witek, B., Stolarczyk, M., Szlósarczyk, M., Kielar, S., Hubicka, U. (2022). Simple, Accurate and Multianalyte Determination of Thirteen Active Pharmaceutical Ingredients in Polypills by HPLC-DAD. Chemosensors, 11(1), 25. https://doi.org/10.3390/chemosensors11010025
- De Diego, M., Godoy, G., Mennickent, S., Olivares, M., Godoy, R. (2010). Stress degradation studies of ramipril by a validated stability-indicating liquid chromatographic method. Journal of the Chilean Chemical Society, 55 (4), 450–453. https://doi.org/10.4067/s0717-97072010000400008
- Typlynska, K., Kondratova, Y., Logoyda, L. (2023). Development of Methods of Quality Control of the Tablets «Ramipril». Scientia Pharmaceutica, 91 (2), 21. https://doi.org/10.3390/scipharm91020021
- The United States Pharmacopeia; The National Formulary (2021). Rockville: United States Pharmacopeial Convention, Inc. Available at: https://www.uspnf.com Last accessed: 22.03.2024
- Al-Majed, A. A., Belal, F., Al-Warthan, A. A. (2001). Spectrophotometric determination of ramipril (a novel ACE inhibitor) in dosage forms. Spectroscopy Letters, 34 (2), 211–220. https://doi.org/10.1081/sl-100002010
- Rahman, N., Ahmad, Y., Azmi, S. N. H. (2005). Kinetic spectrophotometric method for the determination of ramipril in pharmaceutical formulations. AAPS PharmSciTech, 6 (3), E543–E551. https://doi.org/10.1208/pt060368
- Salem, H. (1999). Derivative spectrophotometric determination of two component mixtures. Zhonghuá yáoxué zázhì, 51 (2), 123–142.
- Afieroho, O., Okorie, O., Okonkwo, T. (2012). A Spectrophotometric Method for the Determination of Ramipril in Solid Dosage Forms. Tropical Journal of Pharmaceutical Research, 11 (2), 275–279. https://doi.org/10.4314/tjpr.v11i2.15
- Attimarad, M., Venugopala, K. N., Aldhubiab, B. E., Nair, A. B., SreeHarsha, N., Pottathil, S., Akrawi, S. H. (2019). Development of UV Spectrophotometric Procedures for Determination of Amlodipine and Celecoxib in Formulation: Use of Scaling Factor to Improve the Sensitivity. Journal of Spectroscopy, 2019, 1–10. https://doi.org/10.1155/2019/8202160
- Kumar, M., Jindal, M., Bhatt, S., Pandurangan, A., Malik, A., Kaushik, V. et al. (2019). Simultaneous estimation of amlodipine besylate and ramipril in tablets dosage form by UV spectrophotometric method. Journal of Pharmaceutical Sciences and Research, 11 (2), 667–670.
- Patel, A. B., Jadav, H. M., Vyas, A. J., Patel, A. I., Patel, N. K., Chudasama, A. (2020). Simultaneous determination of ramipril and amlodipine besylate in tablet dosage form by first order derivative spectrophotometric method. Chemical Methodologies, 4 (4), 467–476. https://doi.org/10.33945/sami/chemm.2020.4.8
- Attala, K., Elsonbaty, A. (2021). Smart UV spectrophotometric methods based on simple mathematical filtration for the simultaneous determination of celecoxib and ramipril in their pharmaceutical mixtures with amlodipine: A comparative statistical study. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 244, 118853. https://doi.org/10.1016/j.saa.2020.118853
- Shulyak, N., Protsyk, S., Kuche, T., Kryskiw, L., Poliak, O., Mosula, L., Logoyda, L. (2022). Development of the Spectrophotometric Method for the Determination of Atorvastatin Calcium in Tablets by using Bromophenol Blue. Methods and Objects of Chemical Analysis, 17 (3), 111–117. https://doi.org/10.17721/moca.2022.111-117
- Bromophenol Blue (Compound). 2D Structure. Available at: https://pubchem.ncbi.nlm.nih.gov/compound/Bromophenol-Blue#section=2D-Structure
- Cresol red. Available at: https://pubchem.ncbi.nlm.nih.gov/compound/Cresol-red
- Green Solvent Selection Tool. Available at: https://green-solvent-tool.herokuapp.com/
- State Pharmacopoeia of Ukraine. Vol. 1 (2015). Kharkiv: SE “Ukrainian Scientific Pharmacopoeial Center for Quality of Medicines”, 11148.
- Ermer, J., Agut, C. (2014). Precision of the reportable result. Simultaneous optimisation of number of preparations and injections for sample and reference standard in quantitative liquid chromatography. Journal of Chromatography A, 1353, 71–77. https://doi.org/10.1016/j.chroma.2014.03.043
- Pena-Pereira, F., Wojnowski, W., Tobiszewski, M. (2020). AGREE – Analytical GREEnness Metric Approach and Software. Analytical Chemistry, 92 (14), 10076–10082. https://doi.org/10.1021/acs.analchem.0c01887
- Płotka-Wasylka, J. (2018). A new tool for the evaluation of the analytical procedure: Green Analytical Procedure Index. Talanta, 181, 204–209. https://doi.org/10.1016/j.talanta.2018.01.013
##submission.downloads##
Опубліковано
Як цитувати
Номер
Розділ
Ліцензія
Авторське право (c) 2024 Kateryna Typlynska, Mariana Horyn, Tetyana Kucher, Liubomyr Kryskiw, Liliya Logoyda

Ця робота ліцензується відповідно до Creative Commons Attribution 4.0 International License.
Наше видання використовує положення про авторські права Creative Commons Attribution 4.0 International License для журналів відкритого доступу.
Автори, які публікуються у цьому журналі, погоджуються з наступними умовами:
1. Автори залишають за собою право на авторство своєї роботи та передають журналу право першої публікації цієї роботи на умовах ліцензії Creative Commons Attribution 4.0 International License, котра дозволяє іншим особам вільно розповсюджувати опубліковану роботу з обов'язковим посиланням на авторів оригінальної роботи та першу публікацію роботи у цьому журналі.
2. Автори мають право укладати самостійні додаткові угоди щодо неексклюзивного розповсюдження роботи у тому вигляді, в якому вона була опублікована цим журналом (наприклад, розміщувати роботу в електронному сховищі установи або публікувати у складі монографії), за умови збереження посилання на першу публікацію роботи у цьому журналі.
3. Автори мають право зберігати остаточну прийняту версію статті в інституційному, тематичному або будь-якому іншому репозитарії з метою забезпечення видимості та доступності.







