Дизайн, синтез, молекулярний докінг та антиоксидантні властивості серії нових s-похідних ((1,2,4-триазол-3(2н)-іл)метил)тіопіримидінів
DOI:
https://doi.org/10.15587/2519-4852.2025.312075Ключові слова:
похідні 1,2,4-триазолу, тіопіримідини, молекулярний докінг, DPPH, антиоксидантна активністьАнотація
Метою нашої роботи є синтез нових S-похідних у ряду ((1,2,4-триазол-3(2Н)-іл)метил)тіопіримідинів та дослідження їх антиоксидантної активності з метою виявлення найбільш активних перспективних сполук з використанням молекулярного докінгу та кінетичних параметрів.
Матеріали та методи. ЯМР-спектри 1Н і 13С записані на спектрометрі Bruker AC-500. ВЕРХ записували на системі HPLC Agilent 1260 Infinity, обладнаній діодно-матричним детектором і протонною іонізацією. Елементний аналіз (C, H, N, S) проводили на кубі ELEMENTAR vario EL. Молекулярний докінг проводили за допомогою програми AutoDock 4.2.6. Поглинання вільних радикалів вимірювали за допомогою аналізу вільних радикалів 1,1-дифеніл-2-пікрилгідразилу (DPPH).
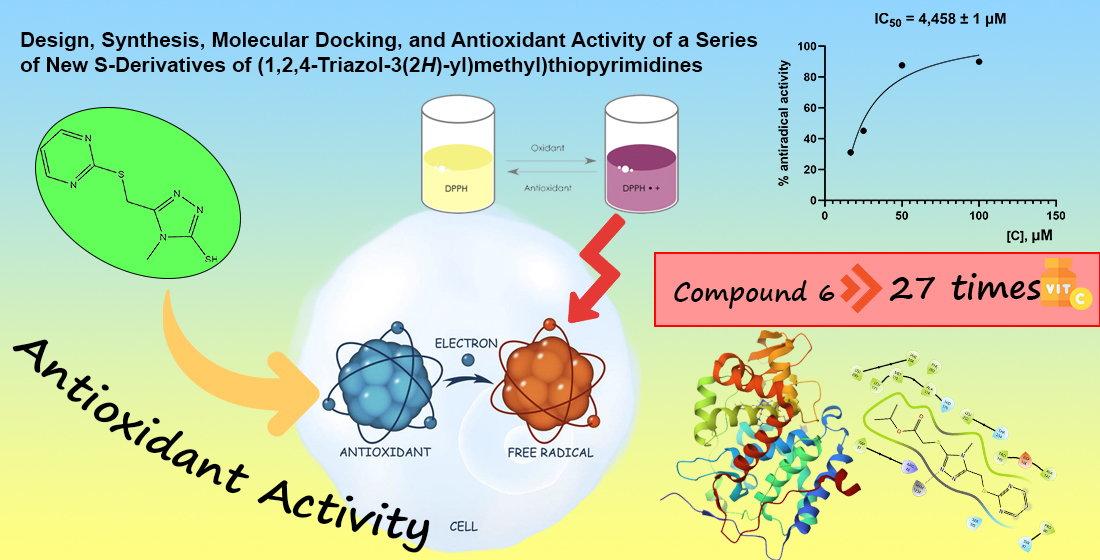
Результати. Шляхом алкілування та подальшої циклізації синтезовано ряд S-ацилпохідних 4-метил-5-((піримідин-2-ілтіо)метил)-4Н-1,2,4-тріазол-3-тіолів. Структуру отриманих сполук підтверджено за допомогою ЯМР-спектроскопії ¹H та ¹³C. Антирадикальну активність оцінювали за допомогою DPPH-тесту, при цьому сполука (6) виявляла найвищу активність, перевершуючи аскорбінову кислоту. Молекулярний докінг із цитохром-с-пероксидазою (PDB: 2X08) підтвердив сильну взаємодію зв’язування, підкреслюючи потенціал цих похідних як антиоксидантів.
Висновки. Три сполуки (1, 6, 8) показали вищу активність, ніж препарат порівняння – природний антиоксидант аскорбінова кислота. Така висока активність може бути пов’язана з наявністю фармакофорних фрагментів, зокрема піримідинового скелета та атома сірки, пов’язаного з 1,2,4-тріазолом. IC50 для найбільш активної сполуки було розраховано як 4,458±1 мкМ, що в 27 разів ефективніше, ніж аскорбінова кислота. Результати молекулярного докінгу показали, що сполуки 4 і 6 мають найнижчу енергію зв’язування, що робить їх найефективнішими сполуками з точки зору антиоксидантної активності
Посилання
- Singh, S. (2024). Antioxidant nanozymes as next-generation therapeutics to free radical-mediated inflammatory diseases: A comprehensive review. International Journal of Biological Macromolecules, 260, 129374. https://doi.org/10.1016/j.ijbiomac.2024.129374
- Olfat, N., Ashoori, M., Saedisomeolia, A. (2022). Riboflavin is an antioxidant: a review update. British Journal of Nutrition, 128 (10), 1887–1895. https://doi.org/10.1017/s0007114521005031
- Ungor, D., Gombár, G., Juhász, Á., Samu, G. F., Csapó, E. (2023). Promising Bioactivity of Vitamin B1-Au Nanocluster: Structure, Enhanced Antioxidant Behavior, and Serum Protein Interaction. Antioxidants, 12 (4), 874. https://doi.org/10.3390/antiox12040874
- Bhatnagar, A., Pemawat, G. (2023). Functionalized Pyrimidines: Synthetic Approaches and Biological Activities. A Review. Organic Preparations and Procedures International, 56 (1), 1–18. https://doi.org/10.1080/00304948.2023.2225385
- Alamshany, Z. M., Nossier, E. S. (2024). New thiazole derivatives linked to pyridine, fused pyridine, pyrimidine and thiazolopyrimidine scaffolds with potential dual anticancer and antimicrobial activities: Design, synthesis and docking simulation. Journal of Molecular Structure, 1316, 138973. https://doi.org/10.1016/j.molstruc.2024.138973
- Bafail, R. S. M., Samman, W. A. (2024). Anti-parkinsonian, anti-inflammatory, anti-microbial, analgesic, anti-hyperglycemic and anticancer activities of poly-fused ring pyrimidine derivatives. Tropical Journal of Pharmaceutical Research, 23 (1), 67–75. https://doi.org/10.4314/tjpr.v23i1.9
- Myriagkou, M., Papakonstantinou, E., Deligiannidou, G.-E., Patsilinakos, A., Kontogiorgis, C., Pontiki, E. (2023). Novel Pyrimidine Derivatives as Antioxidant and Anticancer Agents: Design, Synthesis and Molecular Modeling Studies. Molecules, 28 (9), 3913. https://doi.org/10.3390/molecules28093913
- El-Naggar, M., Hasan, K., Khanfar, M., Shehadi, I. A., El-Awady, R., El-Dein, A. N. et al. (2024). Synthesis, biological assessment and molecular docking study of new sulfur-linked 1,2,4-triazole and 1,2,3-triazole hybrid derivatives as potential DNA gyrase inhibitors. Zeitschrift Für Naturforschung B, 79 (7), 419–429. https://doi.org/10.1515/znb-2024-0012
- Miedviedieva, K. P., Prytula, R. L., Shmatenko, O. P., Bushuieva, I. V., Parchenko, V. V., Kucherenko, L. I., Vasiuk, S. O. (2024). Express quantitative spectrophotometric determination of 2-(((3-(2-fluorophenyl)- 5-thio-4H-1,2,4-triazol-4-yl)imino)methyl)phenol as an active substance of a medicinal product for the treatment of mycoses. Zaporozhye Medical Journal, 26 (1), 59–65. https://doi.org/10.14739/2310-1210.2024.1.291449
- Karpenko, Y., Kusdemir, G., Parchenko, V., Tüzün, B., Taslimi, P., Karatas, O. F. et al. (2023). A biochemistry‐oriented drug design: synthesis, anticancer activity, enzymes inhibition, molecular docking studies of novel 1,2,4-triazole derivatives. Journal of Biomolecular Structure and Dynamics, 42 (3), 1220–1236. https://doi.org/10.1080/07391102.2023.2253906
- Bitounis, D., Jacquinet, E., Rogers, M. A., Amiji, M. M. (2024). Strategies to reduce the risks of mRNA drug and vaccine toxicity. Nature Reviews Drug Discovery, 23 (4), 281–300. https://doi.org/10.1038/s41573-023-00859-3
- Kaplancıklı, Z., Yurttas, L., Turan-Zitouni, G., Özdemir, A., Göger, G., Demirci, F., Mohsen, U. (2013). Synthesis and Antimicrobial Activity of New Pyrimidine-Hydrazones. Letters in Drug Design & Discovery, 1 (1), 76–81. https://doi.org/10.2174/15701808113109990037
- Pachuta-Stec, A. (2022). Antioxidant Activity of 1,2,4-Triazole and its Derivatives: A Mini-Review. Mini-Reviews in Medicinal Chemistry, 22 (7), 1081–1094. https://doi.org/10.2174/1389557521666210401091802
- Karpenko, Yu. V., Panasenko, O. I., Kulish, S. M., Domnich, A. V. (2023). Synthesis and acute toxicity of new S-derivatives (1,2,4-triazole-3(2H)-yl)methyl) thiopyrimidines. Current Issues in Pharmacy and Medicine: Science and Practice, 16 (2), 158–164. https://doi.org/10.14739/2409-2932.2023.2.274586
- Pham, Q. M., Le, T. T. H., Pham, T. H. M., Tran, Q. T., Do, T. L., Vu, T. T. L., Pham, Q. L. (2022). Molecular docking tutorial using AutoDock 4.2.6 on SARS-CoV-2 main protease for beginner. Vietnam Journal of Science and Technology, 60 (6), 929–947. https://doi.org/10.15625/2525-2518/16459
- Murphy, E. J., Metcalfe, C. L., Basran, J., Moody, P. C. E., Raven, E. L. (2008). Engineering the Substrate Specificity and Reactivity of a Heme Protein: Creation of an Ascorbate Binding Site in Cytochrome c Peroxidase. Biochemistry, 47 (52), 13933–13941. https://doi.org/10.1021/bi801480r
- Aallaei, M., Molaakbari, E., Mostafavi, P., Salarizadeh, N., Maleksah, R. E., & Afzali, D. (2022). Investigation of Cu metal nanoparticles with different morphologies to inhibit SARS-CoV-2 main protease and spike glycoprotein using Molecular Docking and Dynamics Simulation. Journal of Molecular Structure, 1253, 132301. https://doi.org/10.1016/j.molstruc.2021.132301
- Gulcin, İ., Alwasel, S. H. (2023). DPPH Radical Scavenging Assay. Processes, 11 (8), 2248. https://doi.org/10.3390/pr11082248
- Gotsulya, A., Fedotov, S., Zinych, O., Trofimova, T., Brytanova, T. (2023). Synthesis and properties of s-alkyl 4-(4-chlorophenyl)-5-(pyrrole-2-yl)-1,2,4-triazole-3-thiol derivatives. Journal of Faculty of Pharmacy of Ankara University, 47 (3), 1020–1032. https://doi.org/10.33483/jfpau.1280492
- Matuszewska, A., Jaszek, M., Stefaniuk, D., Ciszewski, T., Matuszewski, Ł. (2018). Anticancer, antioxidant, and antibacterial activities of low molecular weight bioactive subfractions isolated from cultures of wood degrading fungus Cerrena unicolor. PLOS ONE, 13 (6), e0197044. https://doi.org/10.1371/journal.pone.0197044
##submission.downloads##
Опубліковано
Як цитувати
Номер
Розділ
Ліцензія
Авторське право (c) 2025 Yuriy Karpenko, Kateryna Medvedeva, Andrii Solomennyi, Olga Rudenko, Oleksandr Panasenko, Volodymyr Parchenko, Svitlana Vasyuk

Ця робота ліцензується відповідно до Creative Commons Attribution 4.0 International License.
Наше видання використовує положення про авторські права Creative Commons CC BY для журналів відкритого доступу.







