Розробка нанокомплексів хітозан-ексенатид з жирними кислотами для покращеної доставки пептидів
DOI:
https://doi.org/10.15587/2519-4852.2026.340895Ключові слова:
Ексенатид, хітозан, жирні кислоти, поліелектролітний комплекс (ПЕК)Анотація
Цукровий діабет (ЦД) – поширене ендокринне захворювання, що відповідає за високу захворюваність та смертність у всьому світі. Стандартним медикаментозним лікуванням ЦД є пероральні гіпоглікемічні засоби та/або інсулін. Екзенатид, глюкагоноподібний пептид, використовується для зниження рівня цукру в крові та лікування ЦД протягом останніх 20 років. Застосування екзенатиду обмежується парентеральним шляхом. Розробка пероральної форми екзенатиду є важливим напрямком досліджень, яке забезпечує значні переваги для пацієнтів з діабетом, покращуючи дотримання режиму лікування, зменшуючи навантаження, пов'язане з частими ін'єкціями, та покращуючи результати лікування.
Метою дослідження є приготування ексенатиду як системи пероральної доставки ліків шляхом поєднання переваг наноінкапсуляції з використанням масляного носія з використанням жирних кислот.
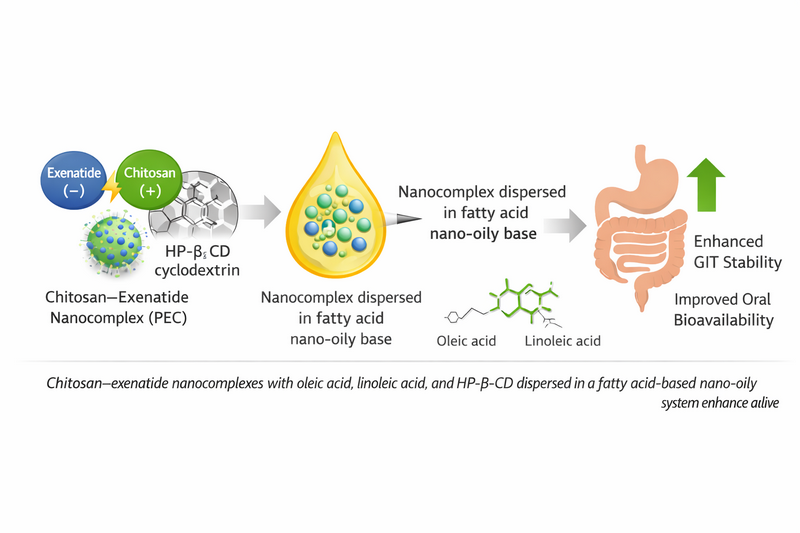
Методи: Для отримання комплексів ексенатид-хітозан (КЕХ) у водному середовищі з метою створення екзенатиду для перорального застосування було використано метод поліелектролітної комплексоутворення. Було досліджено потенціал наночастинок КЕХ-жирних кислот як носіїв ексенатиду для перорального застосування.
Результати: Розміри утворених нанодисперсних частинок відрізнялися при завантаженні розведеним хітозаном або КЕХ. Метод вихрового механічного перемішування дав кращі результати та забезпечив приблизно на 20% кращий захист ексенатиду від шлунково-кишкового тракту, ніж метод механічного перемішування. Результати показали, що гідроксипропіл-β-циклодекстрин (HP-β-CD) мав більш перспективний вплив на формулу олеїнової кислоти (F4), забезпечуючи 87,1% захисту ексенатиду від шлунково-кишкового тракту, але з більшим розміром нанодисперсних частинок 200 нм. Однак, він не дав значно кращих результатів для лінолевої кислоти (F8), яка забезпечила 81,6% захисту шлунково-кишкового тракту та розмір нанодисперсних частинок 210 нм. Дослідження in vivo показало, що формула F4 має Cmax ексенатиду з Tmax 3 години. Рівень глюкози в крові ефективно знижувався до рівня 91 мг/дл протягом 3 годин, зі стійким зниженням до 8 годин.
Висновки: Ексенатид можна захистити від шлунково-кишкових ферментів шляхом включення до лікарського засобу на основі ліпідів хітозану. Метод механічного перемішування з вихровим змішуванням є кращим методом приготування. Використання HP-β-CD покращило захист шлунково-кишкового тракту. Формула F4 є перспективною пероральною альтернативою параентеральному ексенатиду
Посилання
- Shi, Y., Sun, X., Zhang, L., Sun, K., Li, K., Li, Y., Zhang, Q. (2018). Fc-modified exenatide-loaded nanoparticles for oral delivery to improve hypoglycemic effects in mice. Scientific Reports, 8 (1). https://doi.org/10.1038/s41598-018-19170-y
- Yang, J.-M., Wu, L.-J., Lin, M.-T., Lu, Y.-Y., Wang, T.-T., Han, M. et al. (2022). Construction and Evaluation of Chitosan-Based Nanoparticles for Oral Administration of Exenatide in Type 2 Diabetic Rats. Polymers, 14 (11), 2181. https://doi.org/10.3390/polym14112181
- Phan, T. N. Q., Ismail, R., Le-Vinh, B., Zaichik, S., Laffleur, F., Bernkop-Schnürch, A. (2020). The Effect of Counterions in Hydrophobic Ion Pairs on Oral Bioavailability of Exenatide. ACS Biomaterials Science & Engineering, 6 (9), 5032–5039. https://doi.org/10.1021/acsbiomaterials.0c00637
- Aranaz, I., Alcántara, A. R., Civera, M. C., Arias, C., Elorza, B., Heras Caballero, A., Acosta, N. (2021). Chitosan: An Overview of Its Properties and Applications. Polymers, 13 (19), 3256. https://doi.org/10.3390/polym13193256
- Sweidan, K., Jaber, A.-M., Al-Jbour, N., Obaidat, R., Al Remawi, M., Badwan, A. (2011). Further investigation on the degree of deacetylation of chitosan determined by potentiometric titration. Journal of Excipients and Food Chemistry, 2 (1), 16–25.
- Naso, J. N., Bellesi, F. A., Pizones Ruiz-Henestrosa, V. M., Pilosof, A. M. R. (2021). A new methodology to assess the solubility of fatty acids: Impact of food emulsifiers. Food Research International, 139, 109829. https://doi.org/10.1016/j.foodres.2020.109829
- Elsayed, A., Remawi, M. A., Qinna, N., Farouk, A., Badwan, A. (2009). Formulation and characterization of an oily-based system for oral delivery of insulin. European Journal of Pharmaceutics and Biopharmaceutics, 73 (2), 269–279. https://doi.org/10.1016/j.ejpb.2009.06.004
- Ismail, R., Phan, T. N. Q., Laffleur, F., Csóka, I., Bernkop-Schnürch, A. (2020). Hydrophobic ion pairing of a GLP-1 analogue for incorporating into lipid nanocarriers designed for oral delivery. European Journal of Pharmaceutics and Biopharmaceutics, 152, 10–17. https://doi.org/10.1016/j.ejpb.2020.04.025
- Douglas-Gallardo, O. A., Christensen, C. A., Strumia, M. C., Pérez, M. A., Gomez, C. G. (2019). Physico-chemistry of a successful micro-reactor: Random coils of chitosan backbones used to synthesize size-controlled silver nanoparticles. Carbohydrate Polymers, 225, 115241. https://doi.org/10.1016/j.carbpol.2019.115241
- Younes, I., Rinaudo, M. (2015). Chitin and Chitosan Preparation from Marine Sources. Structure, Properties and Applications. Marine Drugs, 13 (3), 1133–1174. https://doi.org/10.3390/md13031133
- Yuan, H., Xiao, P., Wang, F., Guo, C., Pan, S., Jiang, M. et al. (2025). Linoleic acid co-administration promotes oral delivery of exenatide-loaded butyrate-decorated nanocapsules. Journal of Controlled Release, 382, 113744. https://doi.org/10.1016/j.jconrel.2025.113744
- Tekeli, M. C., Aktas, Y., Celebi, N. (2021). Oral self-nanoemulsifying formulation of GLP-1 agonist peptide exendin-4: development, characterization and permeability assesment on Caco-2 cell monolayer. Amino Acids, 53 (1), 73–88. https://doi.org/10.1007/s00726-020-02926-0
- Zulfakar, M. H., Pubadi, H., Ibrahim, S. I., Hairul, N. M. (2024). Medium-Chain Triacylglycerols (MCTs) and Their Fractions in Drug Delivery Systems : A Systematic Review. Journal of Oleo Science, 73 (3), 293–310. https://doi.org/10.5650/jos.ess23204
- Smail, S. S., Ghareeb, M. M., Omer, H. K., Al-Kinani, A. A., Alany, R. G. (2021). Studies on Surfactants, Cosurfactants, and Oils for Prospective Use in Formulation of Ketorolac Tromethamine Ophthalmic Nanoemulsions. Pharmaceutics, 13 (4), 467. https://doi.org/10.3390/pharmaceutics13040467
- Djekic, L., Primorac, M. (2008). The influence of cosurfactants and oils on the formation of pharmaceutical microemulsions based on PEG-8 caprylic/capric glycerides. International Journal of Pharmaceutics, 352 (1-2), 231–239. https://doi.org/10.1016/j.ijpharm.2007.10.041
- Ibrahim, S. A., Li, S. K. (2009). Efficiency of Fatty Acids as Chemical Penetration Enhancers: Mechanisms and Structure Enhancement Relationship. Pharmaceutical Research, 27 (1), 115–125. https://doi.org/10.1007/s11095-009-9985-0
- Mukherjee, S., Shanmugam, G. (2023). A Novel Surfactant with Short Hydrophobic Head and Long Hydrophilic Tail Generates Vesicles with Unique Structural Feature. Small, 19 (19). https://doi.org/10.1002/smll.202206906
- Ribeiro, E. F., de Barros-Alexandrino, T. T., Assis, O. B. G., Junior, A. C., Quiles, A., Hernando, I., Nicoletti, V. R. (2020). Chitosan and crosslinked chitosan nanoparticles: Synthesis, characterization and their role as Pickering emulsifiers. Carbohydrate Polymers, 250, 116878. https://doi.org/10.1016/j.carbpol.2020.116878
- Benamer Oudih, S., Tahtat, D., Nacer Khodja, A., Mahlous, M., Hammache, Y., Guittoum, A., Kebbouche Gana, S. (2023). Chitosan nanoparticles with controlled size and zeta potential. Polymer Engineering & Science, 63 (3), 1011–1021. https://doi.org/10.1002/pen.26261
- Butnaru, E., Stoleru, E., Brebu, M. A., Darie-Nita, R. N., Bargan, A., Vasile, C. (2019). Chitosan-Based Bionanocomposite Films Prepared by Emulsion Technique for Food Preservation. Materials, 12 (3), 373. https://doi.org/10.3390/ma12030373
- Vargas, M., Albors, A., Chiralt, A., González-Martínez, C. (2009). Characterization of chitosan–oleic acid composite films. Food Hydrocolloids, 23 (2), 536–547. https://doi.org/10.1016/j.foodhyd.2008.02.009
- Brunel, F., Véron, L., David, L., Domard, A., Delair, T. (2008). A Novel Synthesis of Chitosan Nanoparticles in Reverse Emulsion. Langmuir, 24 (20), 11370–11377. https://doi.org/10.1021/la801917a
- Eczacioglu, N., Postina, A., Ebert, M., Laffleur, F., Kali, G., Seybold, A., Bernkop-Schnürch, A. (2025). Self-emulsifying drug delivery systems: A comparison of dry and wet reverse micelles. Acta Biomaterialia, 202, 545–558. https://doi.org/10.1016/j.actbio.2025.07.027
- Álvarez-García, S., Couarraze, L., Matos, M., Gutiérrez, G. (2024). Lycopene-Loaded Emulsions: Chitosan Versus Non-Ionic Surfactants as Stabilizers. Molecules, 29 (21), 5209. https://doi.org/10.3390/molecules29215209
- Bowman, K., Leong, K. W. (2006). Chitosan nanoparticles for oral drug and gene delivery. International Journal of Nanomedicine, 1 (2), 117–128. https://doi.org/10.2147/nano.2006.1.2.117
- Claus, V., Spleis, H., Federer, C., Zöller, K., Wibel, R., Laffleur, F. et al. (2023). Self-emulsifying drug delivery systems (SEDDS): In vivo-proof of concept for oral delivery of insulin glargine. International Journal of Pharmaceutics, 639, 122964. https://doi.org/10.1016/j.ijpharm.2023.122964
- Li, H., Zhang, Z., Bao, X., Xu, G., Yao, P. (2018). Fatty acid and quaternary ammonium modified chitosan nanoparticles for insulin delivery. Colloids and Surfaces B: Biointerfaces, 170, 136–143. https://doi.org/10.1016/j.colsurfb.2018.05.063
- Kuroiwa, T., Shino, H., Yoshioka, T., Doi, T., Nishinomiya, T. (2022). Flavor encapsulation into chitosan-oleic acid complex particles and its controlled release characteristics during heating processes. LWT, 167, 113815. https://doi.org/10.1016/j.lwt.2022.113815
- Kurniawan, J., Suga, K., Kuhl, T. L. (2017). Interaction forces and membrane charge tunability: Oleic acid containing membranes in different pH conditions. Biochimica et Biophysica Acta (BBA) – Biomembranes, 1859 (2), 211–217. https://doi.org/10.1016/j.bbamem.2016.11.001
- Boughanmi, R., Oelmann, M., Steinbach, C., Schwarz, S. (2024). Comparative Study on Polyelectrolyte Complex Formation of Chitosan and Pectin or PEMA: Effects of Molecular Weight and Mixing Speed. Polysaccharides, 5 (4), 842–856. https://doi.org/10.3390/polysaccharides5040052
- Tiwari, G., Tiwari, R., Rai, A. (2010). Cyclodextrins in delivery systems: Applications. Journal of Pharmacy And Bioallied Sciences, 2 (2), 72–79. https://doi.org/10.4103/0975-7406.67003
- Zapadka, K. L., Becher, F. J., Gomes dos Santos, A. L., Jackson, S. E. (2017). Factors affecting the physical stability (aggregation) of peptide therapeutics. Interface Focus, 7 (6), 20170030. https://doi.org/10.1098/rsfs.2017.0030
- Musuc, A. M. (2024). Cyclodextrins: Advances in Chemistry, Toxicology, and Multifaceted Applications. Molecules, 29 (22), 5319. https://doi.org/10.3390/molecules29225319
- Kali, G., Haddadzadegan, S., Bernkop-Schnürch, A. (2024). Cyclodextrins and derivatives in drug delivery: New developments, relevant clinical trials, and advanced products. Carbohydrate Polymers, 324, 121500. https://doi.org/10.1016/j.carbpol.2023.121500
- Sarabia-Vallejo, Á., Caja, M. del M., Olives, A. I., Martín, M. A., Menéndez, J. C. (2023). Cyclodextrin Inclusion Complexes for Improved Drug Bioavailability and Activity: Synthetic and Analytical Aspects. Pharmaceutics, 15 (9), 2345. https://doi.org/10.3390/pharmaceutics15092345
- Cid-Samamed, A., Rakmai, J., Mejuto, J. C., Simal-Gandara, J., Astray, G. (2022). Cyclodextrins inclusion complex: Preparation methods, analytical techniques and food industry applications. Food Chemistry, 384, 132467. https://doi.org/10.1016/j.foodchem.2022.132467
- Fonte, P., Nogueira, T., Gehm, C., Ferreira, D., Sarmento, B. (2011). Chitosan-coated solid lipid nanoparticles enhance the oral absorption of insulin. Drug Delivery and Translational Research, 1 (4), 299–308. https://doi.org/10.1007/s13346-011-0023-5
##submission.downloads##
Опубліковано
Як цитувати
Номер
Розділ
Ліцензія
Авторське право (c) 2026 Rana Hani Mohammed Ali Al-Shaikh Hamed, Muhammed Hameed Faeadh Hsn Al-Jumaily

Ця робота ліцензується відповідно до Creative Commons Attribution 4.0 International License.
Наше видання використовує положення про авторські права Creative Commons Attribution 4.0 International License для журналів відкритого доступу.
Автори, які публікуються у цьому журналі, погоджуються з наступними умовами:
1. Автори залишають за собою право на авторство своєї роботи та передають журналу право першої публікації цієї роботи на умовах ліцензії Creative Commons Attribution 4.0 International License, котра дозволяє іншим особам вільно розповсюджувати опубліковану роботу з обов'язковим посиланням на авторів оригінальної роботи та першу публікацію роботи у цьому журналі.
2. Автори мають право укладати самостійні додаткові угоди щодо неексклюзивного розповсюдження роботи у тому вигляді, в якому вона була опублікована цим журналом (наприклад, розміщувати роботу в електронному сховищі установи або публікувати у складі монографії), за умови збереження посилання на першу публікацію роботи у цьому журналі.
3. Автори мають право зберігати остаточну прийняту версію статті в інституційному, тематичному або будь-якому іншому репозитарії з метою забезпечення видимості та доступності.







