Фармакологічна дія густого екстракту квітів пижма звичайного (Tanacetum vulgare L.) на експериментальній моделі естроген-індукованого холестазу
DOI:
https://doi.org/10.15587/2519-4852.2026.359582Ключові слова:
Естроген-індукований холестаз (ЕІХ), щури, густий екстракт квітів Tanacetum vulgare L. (ГЕКПЗ), антиоксидантні властивості, захисний ефектАнотація
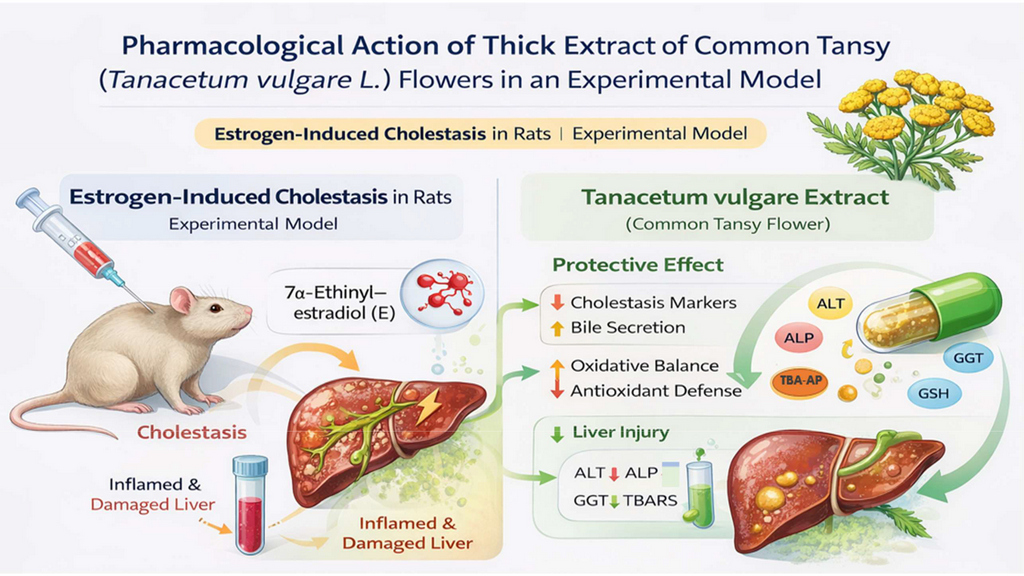
Мета - дослідити протекторний вплив густого екстракту квітів Tanacetum vulgare L. (ГЕКПЗ) на експериментальній моделі естроген-індукованого холестазу (ЕІХ).
Матеріали та методи. ЕІХ відтворювали підшкірним введенням 7α-етинілестрадіолу (E) (5 мг/кг) щурам. ГЕКПЗ та препарат порівняння (ПП) холелесан (ChL) вводили тваринам внутрішньошлунково один раз на добу впродовж трьох діб до та п’яти діб в період моделювання. Через добу після останнього введення Е тварин наркотизували (тіопентал-натрію, 50 мг/кг, внутрішньоочеревинно), визначали об'єм виділеної жовчі за 60 хв і розраховували швидкість жовчовиділення (ШЖ). У сироватці крові визначали активність аланін-амінотрансферази (АлАТ), лужної фосфатази (ЛФ), гамма-глутамілтранспептидази (ГТТ), вміст ТБК-активних продуктів (ТБК-АП) та відновленого глутатіону (ВГ). Для гістологічного дослідження підготовлені зрізи печінки фарбували гематоксиліном, еозином та суданом ΙV для ідентифікації ліпідів. Проводили напівкількісну оцінку ознак ЕІХ.
Результати дослідження. У тварин з ЕІХ ГЕКПЗ сприяв нормалізації показників об'єму та швидкості секреції жовчі до рівня інтактного контролю (ІК), достовірному (р < 0,05) щодо контрольної патології (КП) зниженню досліджуваних показників: АлАТ, ЛФ та ГТТ, зниженню процесів перекисного окислення ліпідів (ПОЛ) та посиленню антиоксидантного захисту печінки, про що свідчить відповідно достовірне зниження рівня ТБК-АП (30,98±0,90 мкмоль/г проти 44,87±4,26, р < 0,05) та підвищення ВГ в 1,9 разів (4,11±0,36 мкмоль/г проти 2,19±0,16, р < 0,05). Загалом ГЕКПЗ виявляв нормалізувальний вплив подібний до ПП, проте поступався йому за впливом на ШЖ та на активність АлАТ і рівень ТБК-АП. Після введення ГЕКПЗ виразність проліферації дуктул вірогідно знизилася у 1,6 рази (р < 0,05), перидуктального запалення у 3,8 рази (р < 0,05), жирової дистрофії гепатоцитів перидуктальних зон у 2,3 рази (р < 0,05) порівняно з КП.
Висновки. Встановлена здатність ГЕКПЗ поліпшувати порушену функцію печінки за умов ЕІХ та знижувати патологічні прояви
Посилання
- Yu, L., Liu, Y., Wang, S., Zhang, Q., Zhao, J., Zhang, H. et al. (2023). Cholestasis: exploring the triangular relationship of gut microbiota-bile acid-cholestasis and the potential probiotic strategies. Gut Microbes, 15 (1). https://doi.org/10.1080/19490976.2023.2181930
- Kolarić, T. O., Ninčević, V., Smolić, R., Smolić, M., Wu, G. Y. (2019). Mechanisms of Hepatic Cholestatic Drug Injury. Journal of Clinical and Translational Hepatology, 7 (1), 86–92. https://doi.org/10.14218/jcth.2018.00042
- Onofrio, F. Q., Hirschfield, G. M. (2020). The Pathophysiology of Cholestasis and Its Relevance to Clinical Practice. Clinical Liver Disease, 15 (3), 110–114. https://doi.org/10.1002/cld.894
- Yu, L., Liu, X., Li, X., Yuan, Z., Yang, H., Zhang, L., Jiang, Z. (2016). Protective effects of SRT1720 via the HNF1α/FXR signalling pathway and anti-inflammatory mechanisms in mice with estrogen-induced cholestatic liver injury. Toxicology Letters, 264, 1–11. https://doi.org/10.1016/j.toxlet.2016.10.016
- Chen, C., Gong, X., Yang, X., Shang, X., Du, Q., Liao, Q. et al. (2019). The roles of estrogen and estrogen receptors in gastrointestinal disease (Review). Oncology Letters, 18 (6), 5673–5680. https://doi.org/10.3892/ol.2019.10983
- Smith, D. D., Rood, K. M. (2020). Intrahepatic Cholestasis of Pregnancy. Clinical Obstetrics & Gynecology, 63 (1), 134–151. https://doi.org/10.1097/grf.0000000000000495
- Mutlu, M. F., Aslan, K., Guler, I., Mutlu, I., Erdem, M., Bozkurt, N., Erdem, A. (2017). Two cases of first onset intrahepatic cholestasis of pregnancy associated with moderate ovarian hyperstimulation syndrome after IVF treatment and review of the literature. Journal of Obstetrics and Gynaecology, 37 (5), 547–549. https://doi.org/10.1080/01443615.2017.1286302
- Mor, M., Shmueli, A., Krispin, E., Bardin, R., Sneh-Arbib, O., Braun, M. et al. (2020). Intrahepatic cholestasis of pregnancy as a risk factor for preeclampsia. Archives of Gynecology and Obstetrics, 301 (3), 655–664. https://doi.org/10.1007/s00404-020-05456-y
- Ma, X., Jiang, Y., Zhang, W., Wang, J., Wang, R., Wang, L. et al. (2020). Natural products for the prevention and treatment of cholestasis: A review. Phytotherapy Research, 34 (6), 1291–1309. https://doi.org/10.1002/ptr.6621
- Wang, R., Cheng, N., Peng, R., Yu, Z., Nan, M., Cao, H. (2020). Oral herbal medicine for women with intrahepatic cholestasis in pregnancy: a systematic review of randomized controlled trials. BMC Complementary Medicine and Therapies, 20 (1). https://doi.org/10.1186/s12906-020-03097-x
- Mishchenko, O. Ya., Hontova, T. M., Yurchenko, K. Yu., Zolotaikina, M. Yu., Herbina, N. A., Ruban, O. A., Kalko, K. O. (2020). Pat. 139684 UA. Analhetychnyi Zasib. MKP (2006) A61K 36/00, A61K 9/02 (2006.01) A61R 29/00. No. u201907609; declareted: 08.07.2019; published:10.01.2020, Bul. No. 1/2020.
- Herbina, N. A., Ruban, O. A., Gontova, T. M., Yaremenko, M. S., Yurchenko, C. Yu. (2021). The study of the qualitative and quantitative content of the amount of flavonoids and hydroxycinnamic acids in a dense extract of common tansy flowers. News of Pharmacy, 2 (102), 8–13. https://doi.org/10.24959/nphj.21.55
- Yurchenko, C., Mishchenko, O., Herbina, N., Каpustyanskiy, I. (2021). Screening study of the choleretic and cholekinetic effects of the the common tansy (Tanacetum vulgare L.) flowers thick extract. Pharmacology and Drug Toxicology, 15 (3), 197–203. https://doi.org/10.33250/15.03.197
- Xu, Y.-J., Yu, Z.-Q., Zhang, C.-L., Li, X.-P., Feng, C.-Y., Lei, K. et al. (2025). CORRIGENDUM: Protective Effects of Ginsenosides on 17α-Ethynyelstradiol-Induced Intrahepatic Cholestasis via Anti-Oxidative and Anti-Inflammatory Mechanisms in Rats. The American Journal of Chinese Medicine, 53 (8), 2603–2604. https://doi.org/10.1142/s0192415x2592003x
- Kholelesan® kapsuly blister No. 30. Compendium. Available at: https://compendium.com.ua/dec/338632/446070/
- Drohovoz, S. M., Hubskyi, Yu. I., Skakun, M. P., Kovalenko, V. M., Derymedvid, L. V. (2001). Eksperymentalne vyvchennia zhovchohinnoi, kholespazmolitychnoi, kholelitiaznoi ta hepatoprotektornoi aktyvnosti novykh likarskykh zasobiv. Doklinichne doslidzhennia likarskykh zasobiv. Kyiv, 334–351.
- European convention for the protection of vertebrate animals used for the experimental and other scientific purposes: European Treaty Series No. 123: Text amended according to the provisions of the Protocol (ETS No. 170), as of its entry into force, on 2 December 2005 (1986). Strasbourg, 48.
- Beutler, E., Duron, O., Kelly, B. M. (1963). Improved method for the determination of blood glutathione. Journal of Laboratory and Clinical Medicine, 61, 882–888.
- Golovanova, I. A., Belikova, I. V., Lyakhova, N. O. (2017). Osnovy medychnoi statystyky. Poltava, 113.
- Crocenzi, F. A., Sánchez Pozzi, E. J., Pellegrino, J. M., Favre, C. O., Rodríguez Garay, E. A., Mottino, A. D. et al. (2001). Beneficial Effects of Silymarin on Estrogen–Induced Cholestasis in the Rat: A Study In Vivo And in Isolated Hepatocyte Couplets. Hepatology, 34 (2), 329–339. https://doi.org/10.1053/jhep.2001.26520
- Zu, Y., Yang, J., Zhang, C., Liu, D. (2021). The Pathological Mechanisms of Estrogen-Induced Cholestasis: Current Perspectives. Frontiers in Pharmacology, 12. https://doi.org/10.3389/fphar.2021.761255
- Kawamura, K., Kobayashi, Y., Kageyama, F., Kawasaki, T., Nagasawa, M., Toyokuni, S. et al. (2000). Enhanced Hepatic Lipid Peroxidation in Patients With Primary Biliary Cirrhosis. American Journal of Gastroenterology, 95 (12), 3596–3601. https://doi.org/10.1111/j.1572-0241.2000.03300.x
- Hussein, M. A. (2013). Prophylactic Effect of Resveratrol Against Ethinylestradiol-Induced Liver Cholestasis. Journal of Medicinal Food, 16 (3), 246–254. https://doi.org/10.1089/jmf.2012.0183
- Mureşana, M., Benedeca, D., Vlasea, L., Opreana, R., Toiua, A., Onigaa, I. (2015). Screening of polyphenolic compounds, antioxidant and antimicrobial properties of Tanacetum vulgare from Transylvania. Studia Universitatis Babes-Bolyai Chemia, 60 (1), 127–138.
- Mishchenko, O., Kyrychenko, I., Gontova, T., Kalko, K., Hordiei, K. (2022). Research on the phenolic profile, antiradical and anti-inflammatory activity of a thick hydroalcoholic feverfew (Tanacetum parthenium L.) herb extract. ScienceRise: Pharmaceutical Science, 5 (39), 91–99. https://doi.org/10.15587/2519-4852.2022.266400
##submission.downloads##
Опубліковано
Як цитувати
Номер
Розділ
Ліцензія
Авторське право (c) 2026 Oksana Mishchenko, Yaroslava Butko, Oksana Tkachova, Olena Khalieieva, Andrii Berezniakov, Oleksii Andriianenkov

Ця робота ліцензується відповідно до Creative Commons Attribution 4.0 International License.
Наше видання використовує положення про авторські права Creative Commons Attribution 4.0 International License для журналів відкритого доступу.
Автори, які публікуються у цьому журналі, погоджуються з наступними умовами:
1. Автори залишають за собою право на авторство своєї роботи та передають журналу право першої публікації цієї роботи на умовах ліцензії Creative Commons Attribution 4.0 International License, котра дозволяє іншим особам вільно розповсюджувати опубліковану роботу з обов'язковим посиланням на авторів оригінальної роботи та першу публікацію роботи у цьому журналі.
2. Автори мають право укладати самостійні додаткові угоди щодо неексклюзивного розповсюдження роботи у тому вигляді, в якому вона була опублікована цим журналом (наприклад, розміщувати роботу в електронному сховищі установи або публікувати у складі монографії), за умови збереження посилання на першу публікацію роботи у цьому журналі.
3. Автори мають право зберігати остаточну прийняту версію статті в інституційному, тематичному або будь-якому іншому репозитарії з метою забезпечення видимості та доступності.







