Identifying the conditions for production of synthetic rutile by leaching of reduced Samotkan ilmenite with ferric sulfate solutions
DOI:
https://doi.org/10.15587/1729-4061.2025.328308Keywords:
Samotkan weathered ilmenite, synthetic rutile, ferric sulfate, hydroxysulphate, recycling, TiO2Abstract
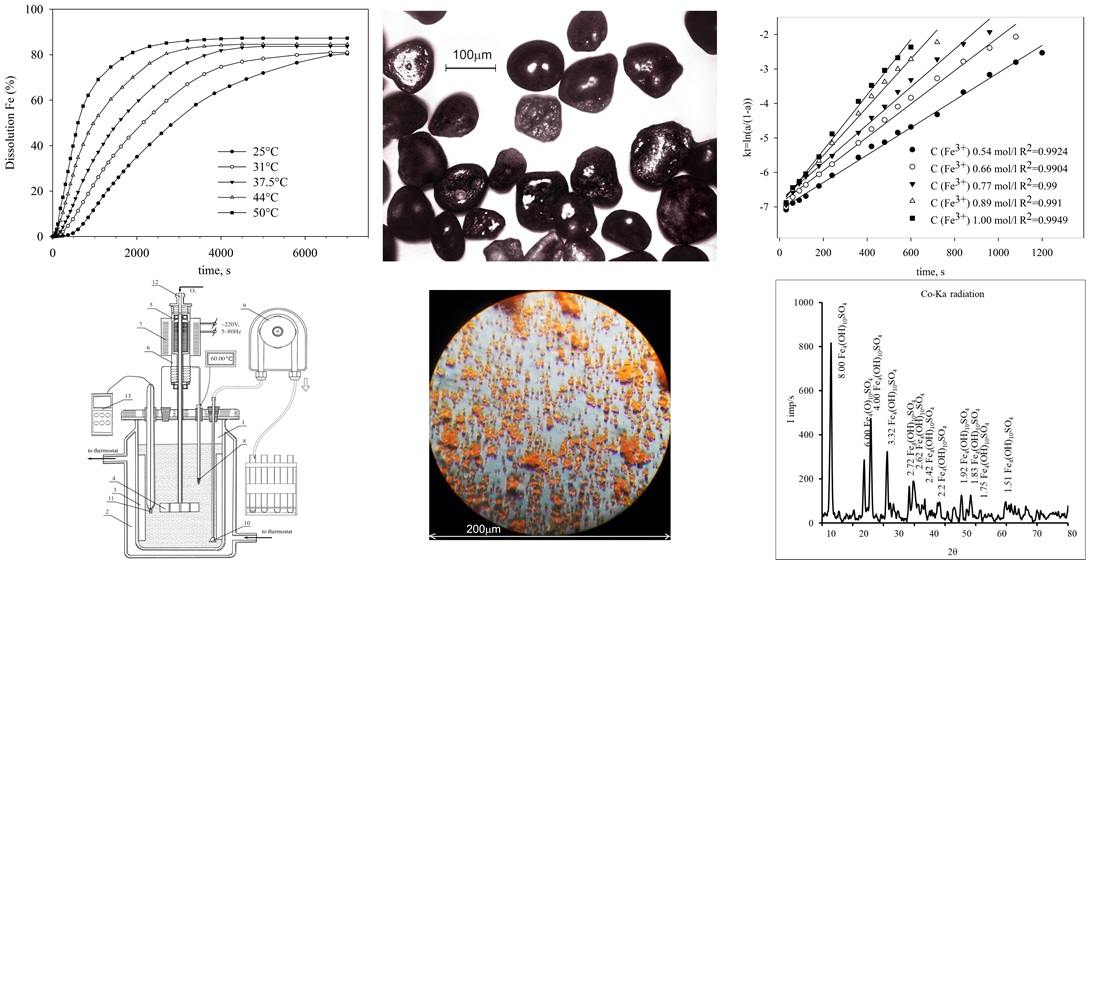
This study investigates the chemical beneficiation processes for Samotkan ilmenite concentrates, reagent regeneration, and the recycling of extracted iron compounds. The task addressed is to devise technology for obtaining synthetic rutile and converting by-product iron compounds into commercially valuable materials. Kinetic parameters of iron leaching from metallized ilmenite obtained by reducing Samotkan ilmenite concentrate with carbon at 1200 ℃ for 4 hours using ferric sulfate solutions were determined. Up to 8 % iron extraction, the kinetics followed the autocatalytic Prout–Tompkins model (kt=ln(a/(1–a)), with apparent activation energy Еapp=62.7 kJ/mol. At higher degrees of iron extraction, the process was consistent with the shrinking core model (kt=1–(1–a)1/3), with apparent activation energy Еapp=47.3 kJ/mol. The reaction order with respect to Fe3+ was found to be close to first order. Additional removal of impurities from the residue of oxidative leaching was achieved by treatment with 15 % H2SO4 solution at 60 ℃ and subsequent calcination at 800 ℃, resulting in the production of synthetic rutile with a ТіО2 content of 92 %. It was established that the regeneration of oxidative leaching solutions could be carried out via catalytic oxidation of FeSO4 solutions using oxygen. At pH 1.1–1.5 and 60 ℃ in the presence of NO, ferrous iron was quantitatively oxidized within 1–3 hours. Efficient mass transfer under high gas content in the gas-liquid mixture allows oxidation to proceed without elevated oxygen pressure or temperature. A portion of the ferric iron was recovered as high-purity crystalline Fe4(OH)10SO4 precipitates, which, upon calcination at 750 ℃, yielded 99.4 % Fe2O3, suitable for pigment production. The low reagent consumption and the conversion of iron into marketable products underscore the potential for industrial-scale implementation of this process
References
- Mineral commodity summaries 2024 (2024). US Geological Survey. https://doi.org/10.3133/mcs2024
- Joy, M., Bhat, K. H. (2025). An overview of phase analysis and strategies on the development of acid soluble titania for sulphate process. Discover Chemistry, 2 (1). https://doi.org/10.1007/s44371-025-00110-5
- Interim Report. For The Half-Year Ended 30 June 2024 (2024). Iluka Resources Limited. Available at: https://www.iluka.com/media/pannp5i3/2024-half-year-results-interim-report.pdf
- Jung, E. J., Kim, J., Lee, Y. R. (2021). A comparative study on the chloride effectiveness of synthetic rutile and natural rutile manufactured from ilmenite ore. Scientific Reports, 11 (1). https://doi.org/10.1038/s41598-021-83485-6
- Middlemas, S. C. (2014). Energy-conscious production of titania and titanium powders from slag. The University of Utah . Available at: https://core.ac.uk/download/276265554.pdf
- Reck, E., Richards, M. (1997). Titanium dioxide – Manufacture, environment and life cycle analysis: The tioxide experience. Surface Coatings International, 80 (12), 568–572. https://doi.org/10.1007/bf02693848
- Zhang, S., Liu, S., Ma, W., Dai, Y. (2018). Review of TiO2-Rich Materials Preparation for the Chlorination Process. Rare Metal Technology 2018, 225–234. https://doi.org/10.1007/978-3-319-72350-1_21
- Ganzha, O., Kuzmanenko, H., Okholina, T., Remezova, O. (2022). Current State Of Mineral Base Of Titanium Deposits Of Ukraine. Visnyk of Taras Shevchenko National University of Kyiv. Geology, 4 (99), 60–66. https://doi.org/10.17721/1728-2713.99.08
- Ganzha, O. A., Kovalchuk, M. S., Kroshko, Yu. V. (2024). Ore-Bearing Of The Vovchansk Zircon-Rutil-Ilmenite Deposit. Geochemistry and Ore Formation, 45, 30–43. https://doi.org/10.15407/gof.2024.45.030
- Filippou, D., Hudon, G. (2009). Iron removal and recovery in the titanium dioxide feedstock and pigment industries. JOM, 61 (10), 36–42. https://doi.org/10.1007/s11837-009-0150-3
- Thambiliyagodage, C., Wijesekera, R., Bakker, M. G. (2021). Leaching of ilmenite to produce titanium based materials: a review. Discover Materials, 1 (1). https://doi.org/10.1007/s43939-021-00020-0
- Lakshmanan, V. I., Bhowmick, A., Halim, A.; Brown, J. (Ed.) (2014). Titanium Dioxide - Production, Properties and Applications. New York: Nova Science, 75–130.
- Walpole, E. A., Winter, J. D. (2002). The Austpac ERMS and EARS Processes for the Manufacture of High-Grade Synthetic Rutile by the Hydrochloric Acid Leaching of Ilmenite. Chloride Metallurgy 2002 – International Conference on the Practice and Theory of Chloride/Metal Interaction. Available at: https://www.austpacresources.com/pdfs/techpub/EJW%20Paper%20Oct%202002.pdf
- Verhulst, D., Sabachy, B., Spitler, T., Duyvesteyn, W. (2002). New development in the Altair hydrochloride TiO2 pigment process. Hydrometallurgy Fifth International Conference in Honor of Professor Ian Ritchie, 565–575.
- Farrow, J. B., Ritchie, I. M., Mangano, P. (1987). The reaction between reduced ilmenite and oxygen in ammonium chloride solutions. Hydrometallurgy, 18 (1), 21–38. https://doi.org/10.1016/0304-386x(87)90014-4
- Shiah, C. D. (1966). Pat. No. US3252787A. Process for prodúcing titanium dioxide concentrate and other useful products from ilmenite and similar ores. Available at: https://patents.google.com/patent/US3252787A/en
- Ward, C. B. (1990). The production of synthetic rutile and by-product iron oxide pigments from ilmenite processing. Materials Science, 309–322.
- Gok, O. (2011). Catalytic oxidation mechanism of oxy-nitrogen species (NOx) in FeSO4 electrolyte. Nitric Oxide, 25 (1), 47–53. https://doi.org/10.1016/j.niox.2011.05.003
- Baldwin, S. A., Van Weert, G. (1996). On the catalysis of ferrous sulphate oxidation in autoclaves by nitrates and nitrites. Hydrometallurgy, 42 (2), 209–219. https://doi.org/10.1016/0304-386x(95)00092-u
- Kozhura, O. V., Tsybulya, E. O., Kovalenko, I. L. (2025). Leaching of reduced ilmenite concentrate from the Samotkan deposit using sulfuric acid solutions. Voprosy Khimii i Khimicheskoi Tekhnologii, 2, 150–157. https://doi.org/10.32434/0321-4095-2025-159-2-150-157
- Lv, W., Lv, X., Xiang, J., Hu, K., Zhao, S., Dang, J. et al. (2019). Effect of preoxidation on the reduction of ilmenite concentrate powder by hydrogen. International Journal of Hydrogen Energy, 44 (8), 4031–4040. https://doi.org/10.1016/j.ijhydene.2018.12.139
- Sarker, M. K., Rashid, A. K. M. B., Kurny, A. S. W. (2006). Kinetics of leaching of oxidized and reduced ilmenite in dilute hydrochloric acid solutions. International Journal of Mineral Processing, 80 (2-4), 223–228. https://doi.org/10.1016/j.minpro.2006.04.005
- House, J. E. (2007). Principles of chemical kinetics. Academic Press, 336.
- Nikiforova, A., Kozhura, O., Pasenko, O. (2016). Leaching of vanadium by sulfur dioxide from spent catalysts for sulfuric acid production. Hydrometallurgy, 164, 31–37. https://doi.org/10.1016/j.hydromet.2016.05.004
- Gok, O. (2012). Ferrous oxidation catalyzed by oxy-nitrogen species (NOX). Asian Journal of Chemistry, 24 (12), 5485–5489. Available at: https://asianpubs.org/index.php/ajchem/article/view/9911
- El-Guindy, M. I., Davenport, W. G. (1970). Kinetics and mechanism of llmenite reduction with graphite. Metallurgical Transactions, 1 (6), 1729–1734. https://doi.org/10.1007/bf02642023
- Rhamdhani, M. A., Ahmad, S., Pownceby, M. I., Bruckard, W. J., Harjanto, S. (2018). Selective sulphidation of impurities in weathered ilmenite. Part 1 – Applicability to different ilmenite deposits and simulated Becher kiln conditions. Minerals Engineering, 121, 55–65. https://doi.org/10.1016/j.mineng.2018.03.005
- Xiang, J., Pei, G., Lv, W., Liu, S., Lv, X., Qiu, G. (2020). Preparation of synthetic rutile from reduced ilmenite through the aeration leaching process. Chemical Engineering and Processing - Process Intensification, 147, 107774. https://doi.org/10.1016/j.cep.2019.107774
- Duong, B. N., Truong, T. N., Nguyen, T. T. (2020). The Upgrading of Ha Tinh Ilmenite to Synthetic Rutile by Becher Process. Materials Science Forum, 985, 115–123. https://doi.org/10.4028/www.scientific.net/msf.985.115
- Abdelgalil, M. S., El-Barawy, K., Ge, Y., Xia, L. (2023). The Recovery of TiO2 from Ilmenite Ore by Ammonium Sulfate Roasting–Leaching Process. Processes, 11 (9), 2570. https://doi.org/10.3390/pr11092570
- Matijević, E., Sapieszko, R. S., Melville, J. B. (1975). Ferric hydrous oxide sols I. Monodispersed basic iron(III) sulfate particles. Journal of Colloid and Interface Science, 50 (3), 567–581. https://doi.org/10.1016/0021-9797(75)90180-0
Downloads
Published
How to Cite
Issue
Section
License
Copyright (c) 2025 Oleg Kozhura, Yevhen Tsybulia, Alona Derimova, Viktoriia Yaroshenko

This work is licensed under a Creative Commons Attribution 4.0 International License.
The consolidation and conditions for the transfer of copyright (identification of authorship) is carried out in the License Agreement. In particular, the authors reserve the right to the authorship of their manuscript and transfer the first publication of this work to the journal under the terms of the Creative Commons CC BY license. At the same time, they have the right to conclude on their own additional agreements concerning the non-exclusive distribution of the work in the form in which it was published by this journal, but provided that the link to the first publication of the article in this journal is preserved.
A license agreement is a document in which the author warrants that he/she owns all copyright for the work (manuscript, article, etc.).
The authors, signing the License Agreement with TECHNOLOGY CENTER PC, have all rights to the further use of their work, provided that they link to our edition in which the work was published.
According to the terms of the License Agreement, the Publisher TECHNOLOGY CENTER PC does not take away your copyrights and receives permission from the authors to use and dissemination of the publication through the world's scientific resources (own electronic resources, scientometric databases, repositories, libraries, etc.).
In the absence of a signed License Agreement or in the absence of this agreement of identifiers allowing to identify the identity of the author, the editors have no right to work with the manuscript.
It is important to remember that there is another type of agreement between authors and publishers – when copyright is transferred from the authors to the publisher. In this case, the authors lose ownership of their work and may not use it in any way.